Imunostimulirajući konjugati antitijela izazivaju snažnu mijeloičnu aktivaciju i izdržljivi antitumorski imunitet (2. dio)
Jun 17, 2022
Za više informacija kontaktirajtedavid.wan@wecistanche.com
Rasprava:
Ovdje predstavljeni rezultati pružaju uvjerljive dokaze koji podržavaju ISAC kao novu tehnologiju za imunoterapiju tumora. In vitro modeliranje ISAC-ova pokazalo je njihovu sposobnost da aktiviraju primarne ljudske mijeloične APC-ove na način ovisan o Fc R i TLR-u i da poboljšaju unakrsnu prezentaciju antigena korištenjem modela mišjeg OVA sustava. Aktivacija putem pojačane regulacije kostimulacijske molekule CD40 nije opažena samo in vitro, već je također viđena na mijeloidnim APC-ima koji se nalaze u tumorima u modelima ksenografta i singenih tumora. Jedno od upečatljivih otkrića ove studije bilo je da je kovalentno vezanje agonista TLR-a na tumor-ciljano monoklonsko protutijelo u obliku ISAC-a promijenilo je imunostimulacijski ishod i ukupnu učinkovitost koja se obično očekuje s TLR agonistima. Usporedba lokalne primjene trastuzumaba u kombinaciji s T785 sa sustavnom isporukom T785-ISAC-a pokazala je da je samo ISAC bio uspješan u smanjenju opterećenja tumorom. Lokalna isporuka smjese nije dala nikakvu korist u modelu ksenografta tumora HCC1954, s učincima usporedivim s učinkom samog trastuzumaba. Ovaj nalaz potvrđuje da je ne samo lokalna isporuka, već i istodobna isporuka protutijela i agonista TLR-a ključna za terapeutsku učinkovitost promatranu s ISAC-om. Podaci o mehanizmu generirani u modelu ksenografta tumora HCC1954 pokazali su in vivo zahtjeve za uključenjem Fc R i angažmanom TLR za učinkovitost, jer ni TLRnull-ISAC ni Fc-neaktivni ISAC nisu uspjeli kontrolirati rast tumora. Nadalje, sustavna primjena ISAC-a rezultirala je održivom antitumorskom učinkovitošću u štakorskim HER2 plus singenim modelima tumora i ljudskim HER2 plus ksenograftima raka dojke koji su bili otporni na liječenje nekonjugiranim protutijelima. HER2 je odabran kao ciljni antigen za pretkliničke in vivo studije jer neoadjuvantnom, adjuvantnom i prvom linijom terapije za bolesnice s lokalno uznapredovalim ili metastatskim rakom dojke dominiraju ciljana antitijela na HER2- koja nisu dizajnirana da stimuliraju imunološki sustava i odobrenih inhibitora kontrolnih točaka T stanica koja blokiraju antitijela bila su minimalno učinkovita u ovih bolesnika. Ovi pacijenti bi mogli imati koristi od ISAC-ova koji zadržavaju funkcionalnost matičnih protutijela i dodaju značajan imunostimulacijski potencijal. Kao i kod svakog drugog imunoterapeutika, postoji mogućnost stvaranja ili pogoršanja antitijela protiv lijeka i, u slučaju ISAC-a, može u konačnici ovisiti o imunogenosti matičnog antitijela. Te se procjene najbolje izvode klinički, a trastuzumab bi mogao biti idealan za ispitivanje budući da je prijavljena stopa imunogenosti Herceptina™ kod pacijenata manja od 1 posto. In vivo podaci koji demonstriraju zahtjev za istodobnu isporuku antitijela i adjuvansa dodatno su podržani radom koji detaljno opisuje intracelularnu signalizaciju koja upravlja aktivnošću ISAC kroz simultanu Fc R i TLR signalizaciju. Dok dodatne studije mogu dodatno razjasniti unutarstaničnu dinamiku signalizacije ISAC-a, studije opisane ovdje ističu potencijalne signalne prednosti konjugacije TLR agonista s antitijelom, kao što se obično opaža kada antitijela zahvate patogene tijekom zaštitnog imuniteta. Analiza intracelularne signalizacije zasnovana na CyTOF-u ljudski PBMCs je korišten za daljnjerazumjeti i razlikovati aktivnost smjese i ISAC-a. Rezultati su otkrili pojačani potpis nakon stimulacije ISAC-om u usporedbi s onim izazvanim mješavinom pojedinačnih komponenti, dodatno podupirući potencijal za poboljšanje aktivnosti kroz kemijsku konjugaciju protutijela i TLR agonista. Dok se TLR7 i TLR8-specifična snaga ISAC-ova ne može mjeriti pomoću HEK293 reporterskih stanica, demonstracijafosforilacije IRF-a-7 izazvane ISAC-om sugerira aktivni agonizam TLR7/8, jer je poznato da je IRF-7 nizvodno od TLR7 i TLR8 MyD88-pokrenute signalizacije 30. Podaci pokazuju da ISAC ne samo da izaziva povećanu signalizaciju kanonskih putova povezanih s putevima TLR i Fc R, već također smanjuje prag aktivacije parova koji je potreban za pokretanje fosforilacije nizvodno signalizirajućih proteina kao što je ribosomalni protein S6, ključni regulator translacije proteina u stanici. Visoki DREMI rezultati, posebno izmjereniu monocitima, kao i u DC-ovima, podupiru jaku uvjetnu ovisnost izazvanu stimulacijom s ISAC-om koja se ne vidi u mješavini. Ovaj fenomen možebiti olakšan unutarstaničnim promjenama u obilju, lokalizaciji i/ili regrutiranju receptora unutar endosoma, no potrebna su daljnja istraživanja kako bi se potvrdio točan mehanizam. Važno je da je DREMI analiza identificirala odnose koji su u skladu s poznatim signalnim partnerima kao rezultat ISAC stimulacije. Svojim poznatim inhibitornimulogu u kanonskom NF-κB signaliziranju 49, uočili smo smanjenu ovisnost (tj. DREMI rezultat)između pIRF7 i inhibitora kapa B (IκB) kada su mijeloidne stanice stimulirane ISAC-om. Zajedno, ovi rezultati podupiru pojačan i održiv intracelularni odgovor preko relevantnih molekula puta prijenosa signala nizvodno od ISAC stimulacije uz sinergiju između signalnih putova povezanih s TLR i Fc R.

Kliknite ovdje da saznate više o Cistancheu
Naši rezultati su otkrili da su funkcionalne Fc-Fc R interakcije bitne za ISAC-posredovanu aktivaciju mijeloidnih APC-ova. Nativni IgG1 Fc, koji ima najveći afinitet za aktiviranje Fc Rs od prirodno postojećih IgG izotipova, bio je superiorniji od drugih IgG izotipova s nižim afinitetima za aktiviranje Fc Rs. Daljnje pojačanje Fc-Fc R interakcije putem fukozilacije povećalo je snagu, dok je smanjenje Fc-Fc R interakcije putem glikozilacije smanjilo snagu. Kao što se očekivalo, Syk signaliziranje nizvodno od Fc R angažmana uz naknadni TLR agonizam bio je potreban da bi ISAC-ovi izazvali maksimalnu stimulaciju. Ove nalaze podupiru studije koje pokazuju dramatično poboljšanje mijeloične stimulacije nakon kostimulacije IgG-om vezanim za ploču i agonistom TLR-a PAM3CSK 50. Oni također sugeriraju da opsežnije umrežavanje Fc, na površini ciljne stanice ili unutar in vitro postavke ploče , ili su uključene diferencijalne signalne mreže, nakon ISAC stimulacije za razliku od mješavine komponenti. Prijevod ISAC platforme in vivo prvi je put procijenjen s humanim HER2 plus tumorskim staničnim linijama kod miševa kojima nedostaju potpuno funkcionalne B, T i NK stanice. Zanimljivo je da je trastuzumab ISAC bio značajno učinkovitiji od trastuzumaba u višestrukim tumorima s različitim razinama ekspresije HER2. Nadalje, podaci su pokazali ovisnost o ciljanju tumora za antitumorske učinke ISAC-a, budući da izotip-ISAC nije mogao potaknuti regresiju i uklanjanje tumora. Iako je in vitro modeliranje pokazalo potrebu za aktivnošću TLR i Fc R kako bi se omogućila moć ISAC-a, takvi modeli nisu bili uspješni u mjerenju ovisnosti o ciljanju ISAC antigena. Nisu izmjerene razlike između ciljanih i izotipa T785-ISAC-ova u testovima na ploči s kokultiviranim mijeloidnim APC-ovima zdravih ljudis tumorskim stanicama (podaci nisu prikazani).Nedostatak ovisnosti o meti izmjeren in vitro može se pripisati višestrukim čimbenicima: utvrđeno je da mijeloidni APC pojačavaju Fc Rs na površini stanice nakon kulture in vitro, što može povećati sposobnost topljivog IgG da se veže na Fc R, što dovodi do pojačani signal iz izotipa ISAC.Dodatno, kulturansustavu nedostaje endogeni IgG i dodatni faktori u serumu prisutni in vivo koji se mogu natjecati za Fc R in vivo i ublažiti učinke uočene s izotipom ISAC.Bez obzira na to, in vivo modeli pokazali su ISAC-ovo oslanjanje na ciljanje tumora za antitumorsku učinkovitost.Ne samo da su izotipovi ISAC pokazali mali utjecaj na rast tumora u studijama učinkovitosti, već je također utvrđeno da ne induciraju nikakav utjecaj na genetsku razinu u tumorima, kao što je prikazano u modelima ksenografta i singenih tumora.Uz demonstraciju ciljno ovisne učinkovitosti in vivo, T785-ISAC su tolerirale životinje i inducirao je minimalni gubitak težine, pokazujući malo znakova učinaka izvan cilja i štetnih događaja kod miševa.Ovi podaci dalje podupiru sposobnost sustavno isporučenog ISAC-a koji cilja tumor da putuje do tumora i inducira lokalizirani proupalni antitumorski odgovor.
Važnost efektorskih funkcija posredovanih mijeloidnim stanicama prikazana je u studijama iscrpljivanja stanica, u kojima je smanjenje fagocita klodronatom umanjilo sposobnost ISAC-a da inducira uklanjanje tumora.Zanimljivo, iako su tumori u početku regresirali nakon iscrpljivanja Gr1 pozitivnih stanica, tumori su kasnije izrasli.Ovaj se fenomen mogao pojaviti kao rezultat iscrpljivanja prekursora fagocita kao što su monociti, koji su se kasnije mogli diferencirati u funkcionalne i zrele fagocitne stanice 51.Daljnji molekularni i stanični uvidi dobiveni su kvantificiranjem razina mRNA i promjena nakon tretmana ISAC-om.Ti su podaci dodatno potkrijepljeni imunohistokemijom kao i kvantifikacijom proteina, što ukazuje na infiltraciju mijeloidnih stanica u tumor dužs proizvodnjom proupalnog citokina TNF i mijeloidnih kemoatraktanata CCL2 (MCP-1) i CCL4 (Mip1b).



Slika 2: ISACS izaziva različite signalne obrasce u mijeloidnim APC-ima. (ad) Svježe izolirani ljudski PBMC stimulirani su s 1 μM rituksimab-ISAC-a ili ekvimolarnim ekvivalentom smjese u prisutnosti CD20 plus Toledo tumorskih stanica u omjeru 1:1 omjeru 15 minuta. (a) Srednji arcsinh omjer ISAC-a u odnosu na signaliziranje izmjeren je nakon stimulacije mješavine za različite fosfoproteine kao što je prikazano toplinskom kartom, sa žutom bojom koja označava povećanu signalizaciju, a plavom bojom smanjeni signal. (b) Reprezentativni dijagrami protočne citometrije za pIRF7 i pRPS6 u monocitima i cDC-ima. (c) Višestruka promjena inducirane signalizacije izračunata je kao arcsinh omjer u odnosu na nestimuliranu kontrolu. Fosforilacija IRF7 i ERK1/2 mjerena je u monocitima i cDC-ima nakon stimulacije ISAC-om ili mješavinom. Podaci su iz jednog eksperimenta sa šest donora (srednja vrijednost i SEM); *P<0.05,><0.01,><0.001,><0.0001. (d)="" representative="" drevi="" plots="" following="" dremi="" analysis="" with="" the="" area="" under="" the="" curve="" (auc)="" and="" inflection="" point="" (ip)="" denoted.="" drevi="" plots="" were="" visually="" inspected="" for="" curve="" fit="" and="" signal-to-noise,="" and="" inflection="" points="" were="" calculated="" for="" those="" with="" proper="" sigmoidal="" curve="" fits="" (n/a="" indicates="" no="" curve="">
Receptori za CCL2 i CCL4, CCR2 i CCR5 izraženi su na monocitima i makrofagima, respektivno, što sugerira da bi se ti tipovi stanica mogli regrutirati u tumore tretirane ISAC-om.Nadalje, Cxcl9 i Cxcl11 mRNA, koje kodiraju kemokine specifične za T stanice i koje eksprimiraju DC-ovi u TME-u, također su pojačane liječenjem trastuzumabom ISAC (dodatna slika 23) 52,53.Trastuzumab ISAC s povećanom snagom, uz upotrebu agonista CL264, pokazao je poboljšanu učinkovitost u tumorskim modelima koji su manje eksprimirali HER2.Ovo je važno s obzirom na to da pacijenti čiji tumori izražavaju nizak HER2 imaju ograničenije mogućnosti liječenja i nisu podobni za trastuzumab ili druge terapije koje sadrže trastuzumab.Prolazni gubitak težine od oko 5-10 posto i povećano sustavno izlučivanje TNF-a primijećeni su kod životinja liječenih i ciljanim i izotipskim CL264-ISAC-ovima, što ukazuje na moguće neciljane učinke uz jake anti- uočena aktivnost tumora.Skupni podaci predstavljeni u modelima ksenotransplantata sugeriraju da je fagocitoza posredovana ISAC-om učinkovit mehanizam za uklanjanje tumora, ali bi se ovaj mehanizam mogao poboljšati nakon antigenske prezentacije tumorskih neoantigena T stanicama u imunokompetentnim domaćinima.U tu svrhu, sposobnost ISAC-ova da promiču antitumorsku imunost kod miševa divljeg tipa ispitana je s anti-rHER2 ISAC-ovima u dva različitarHER2-ekspresiju singenih modela (MMC i CT26-rHER2). I T785 i CL264 koji sadrže ISAC procijenjeni su u singenskom MMC modelu s obzirom na visoku ekspresiju antigena rHER2, budući da se pretpostavlja da su ISAC s nižom i većom potencijom učinkoviti s visokom gustoćom antigena na tumorskoj stanici. Oba rHER2 ISAC-a dovela su do potpunog uklanjanja tumora kod životinja koje nose velike tumore (350-950 mm3) u MMC modelu, dok nekonjugirano protutijelo nije uspjelo kontrolirati rast tumora. Analiza razina transkripta mRNA u modelu MMC otkrila je dramatičnu promjenu u regulacijimnogo gena 24 sata nakon tretmana s ciljanim rHER2 T785-ISAC u odnosu na rHER2 antitijelo ili izotip ISAC, uključujući unutar gena uključenih u biologiju mijeloičnih stanica, biologiju TLR i adaptivne imunološke odgovore. Imunohistokemijom su uočeni povećani infiltrati stanica koje eksprimiraju CD11c- i F4/80-, slično trendu uočenom u modelu tumora ksenografta HCC1954. Nadalje, uočena je infiltracija CD8 T stanicaimunohistokemija, podržavajući stvaranje adaptivnog imunološkog odgovora nakon liječenja ISAC-om.
Uz pokazanu važnost fagocita u modelu ksenotransplantata, studije deplecije u modelu MMC singenog tumora otkrile su jaku ovisnost o fagocitima, budući da je deplecija korištenjem liposoma napunjenih klodronatom zaustavila antitumorske učinke posredovane ISAC-om. Štoviše, singenske studije pokazale su ključnu ulogu T stanica u učinkovitosti ISAC-a. Čišćenje tumora izazvano ISAC-om uvelike je ovisilo o aktivnosti CD8 T stanica, budući da je smanjenje CD8 T stanica inhibiralo antitumorsku učinkovitost. Podaci sugeriraju da je aktivnost T stanica vođena TLR-posredovanom aktivacijom mijeloidnih stanica stimuliranih ISAC-om. Takav zahtjev za T-stanice, vjerojatno povezan s prezentacijom antigena povezanih s tumorom od strane ISAC-stimuliranih mijeloidnih stanica, podržava da ISAC-ovi vjerojatno posreduju u njihovoj antitumorskoj aktivnosti kroz najmanje dva mehanizma: fagocitozom i prezentacijom antigena. Dok fagociti daju rani antitumorski odgovor nakon liječenja ISAC-om, antigensko primanje T stanica u konačnici osigurava uklanjanje tumora i trajne učinke izmjerene u potpuno imunokompetentnim modelima. Ova bi kombinacija bila vrlo poželjna za pacijente s rakom jer bi liječenje ISAC-om moglo dovesti do snažnog i trajnog antitumorskog imuniteta. Da bi se dodatno istražila važnost aktivacije T stanica posredovane ISAC-om, miševi su izliječeni od CT26- rHER2 tumora nakon rHER2 CL 264-Liječenje ISAC-om ponovno je pokrenuto, nakon 30 dana nakon što je bilo bez tumora, s roditeljskom staničnom linijom CT26 koja ne izražava rHER2. rHER2-CT26 izliječene životinje bile su zaštićene od izazova s CT26, dok tumorski naivne životinje nisu mogle odbaciti rast tumora. Dodatno, kako bi se pokazalo da je zaštita specifična za staničnu liniju tumora CT26, 4T1 je istovremeno implantiran u kontralateralni bok roditeljskih miševa zaraženih CT26. Iako CT26 tumori nisu uspjeli narasti u her-CT26 izliječenih miševa, rast tumora 4T1 bio je neopterećen i stoga pruža dokaz da je imunitet specifičan za antigen i ovisan o adaptivnom imunološkom odgovoru. Nadalje, ove studije sugeriraju da ISAC-ovi usmjereni na tumor posreduju u imunološkom pamćenju ne samo na početno ciljani tumorski antigen, već i na neciljane antigene. Ovi podaci također sugeriraju da mijeloične stanice mogu predstavljati antigene povezane s tumorom koji pokreću dodatne CTL odgovore. Implikacije ovih nalaza pokazuju da, čak i ako je ciljni tumorski antigen naknadno smanjen ili se ne može vezati na ISAC, imunološka memorija je već aktivirana i sposobna je održati trajan odgovor. Ovaj odgovor nijeograničeno na antigen koji cilja ISAC, ali i na dodatne, neidentificirane antigene izražene tumorom.Uzeti zajedno, ovi podaci pokazuju da ISAC-ovi izazivaju kvalitativno i kvantitativno različitu biologiju koja se odnosi na staničnu aktivaciju i prezentaciju antigena, proliferaciju T stanica i trajni antitumorski imunitet.

Methods and Materials: Antibody Conjugation & Characterization For conjugation of adjuvants to the antibody, adjuvants were first synthesized to include a linker flanked by a reactive group. Conjugates produced using two-step methods were first synthesized through the modification of mAb lysine residues with a heterobifunctional crosslinker SATA. Deprotection of the acetylated thiol exposed a reactive thiol which was then reacted at room temperature for 2-4 hours with an adjuvant-linker flanked by a thio-reactive maleimide. For constructs produced using a single-step conjugation method, TFP esters were then conjugated to an IgG1 antibody. The TFP esters were dissolved in anhydrous DMSO to make a 20 mM stock solution and 5-10 molar equivalents (relative to the antibody) were added to the IgG antibody at 10 mg/mL in PBS. The conjugation reaction was performed at 4-40°C for 2-12 hours. The resulting immunoconjugates were buffer exchanged into PBS (pH 7.4) through desalting (Zeba Columns, Thermo Fisher Scientific) or dialysis to remove excess small molecular weight impurities. The final protein concentration was determined by measuring the absorbance at 280 nm on a Nanodrop 1000 spectrophotometer (Thermo Fisher Scientific). The yields were >75 posto na temelju obnovljenih proteina. SEC analiza otkrila je minimalnu prisutnost agregata, a DAR je određen LC/MS analizom. Pročišćeni ISAC filtrirani su kroz 0.2 μm sterilni filter i pohranjeni na -20 stupnjeva do upotrebe. HEK reporter test HEK293 reporterske stanice koje eksprimiraju ljudski TLR7 ili ljudski TLR8 kupljene su od Invivogena (hub-htlr7 ili hub-htlr8) i protokoli dobavljača su slijedili za staničnu reprodukciju i eksperimentiranje. Ukratko, stanice su uzgajane do 80-85 postotne konfluencije pri 5 posto CO2 u DMEM-u s dodatkom 10 posto FBS-a, Zeocina i Blasticidina. Stanice su zatim nasađene u ravne ploče s 96-jažicama 4x104 stanica/jažici sa supstratom koji sadrži HEK medij za detekciju i imunostimulirajuće molekule. Aktivnost je mjerena upotrebom čitača ploče na 620-655 nm valnoj duljini. Biacore analiza Njegovi proteini Fc gama receptora (FCGR) s oznakom dobiveni su od R&D Systems (FCGR1 (CD64, kat. br. 1257-FC{{23}) }), FCGR2A (CD32a, br. kat. 1257-FC-050), FCGR2B (CD32b, br. kat. 1875-FC-050), FCGR3A (CD16a, br. kat. {{34 }}FC-050). Analiza vezanja provedena je na instrumentu Biacore T200 u HBS-EP plus puferu (GE BR100669) pomoću CM5 čipa (GE BR100530) koji sadrži imobilizirano anti-HIS protutijelo (HIS Capture kit, GE 28995056 ). Rituximab ili Rituximab-ISAC ubrizgani su preko protočnih ćelija koje sadrže uhvaćene FCGR-ove ili samo referentna površinska anti-His protutijela. Podaci su dvostruko referencirani santi-His površina i injekcija samo pufera. Korištena je metoda kinetičke titracije, a površine su regenerirane između ciklusa injekcijom 10 mM glicina, pH 1,5. Podaci su prilagođeni pomoću softvera za procjenu Biacore T200 (V3.1) korištenjem kinetičkog prilagođavanja (1:1) za FCGR1 i FCGR3A (prosjek od 6 izvođenja) i afiniteta u stabilnom stanju (1:1) za FCGR2A i FCGR2B (prosjek od 3 izvođenja). ).
Human Myeloid APC Isolation Myeloid APCs, which predominantly consisted of monocytes (>95%), were isolated from the whole blood of healthy donors (Stanford Blood Center) by density gradient centrifugation using a RosetteSep Human Monocyte Enrichment Cocktail (Stem Cell Technologies). Myeloid APCs were further isolated using a negative selection Human Monocyte Enrichment Kit without CD16 depletion (Stem Cell Technologies) to a final purity of >90 posto utvrđeno protočnom citometrijom na temelju ekspresije CD14, CD16, CD11c i HLA-DR. Priprema Toledo tumorskih stanica Toledo stanice (ATCC) uzgajane su u mediju koje je preporučio dobavljač i održavane su na gustoći stanica koju je preporučio dobavljač (ATCC). Stanice su uklonjene iz kulture, isprane i resuspendirane u PBS s 2 posto FBS i 2 mM EDTA na 1-10x106 stanica/mL. U nekim su slučajevima stanice naknadno obilježene s 2 µM CFSE tijekom 2 minute, a zatim su jednom isprane s RPMI-1640 (Lonza) uz dodatak 10 posto FBS-a (Atlanta Biologicals) i 100 U/mL Pen/Strep (Lonza). Stanice su zatim fiksirane u 2 posto paraformaldehida i isprane tri puta s PBS-om prije daljnje upotrebe. Ispitivanja stanične aktivacije PBMC ili izolirani monociti stavljeni su na 3x105 odnosno 2x105 stanica po jažici, u ploče s ravnim dnom, 96-jažice u IMDM nadopunjen s 10 posto FBS (Atlanta Biologicals), 1 mM natrijevog piruvata (Lonza), 100 μM neesencijalnih aminokiselina (Lonza) i 100 U/mL Pen/Strep (Lonza). Za eksperimente kokulture monocita i tumora, monociti su uzgajani s fiksiranim alogenim tumorskim stanicama u omjeru 3 prema 1. Stanice su zatim inkubirane s imunostimulirajućim sredstvima ili kontrolama 18-36 sati na 37 stupnjeva s 10 posto CO2. Stanična aktivacija mjerena je ekspresijom aktivacijskih markera na površini stanice i proizvodnjom citokina. Razine ekspresije površinskog markera mjerene su protočnom citometrijom s protutijelima protiv CD40 (5C3, BD), CD86 (IT2.2, BD), HLA-DR (L243, BD) i CD16 (3G8, BD), CD14 (MΦP9, BD) i CD123 (7G3, BD). PBMC su analizirani protočnom citometrijom s antitijelima protiv gore navedenih aktivacijskih markera, kao i loza markera CD19 (HIB19, BD), CD56 (B159, BD), CD3 (SK7, BD), CD4 (OKT4, BioLegend), CD8 (SK1, BD) i CD69 (FN50, BD). U svim slučajevima, supernatant stanične kulture sakupljen je nakon 18 ili 36-satne inkubacije, a proizvodnja citokina je mjerena korištenjem kompleta citokinskih kuglica (Human Inflammatory Cytokine Kit, BD Biosciences) i ELISA (TNF Human ELISA kit, eBiosciences) .Masovana citometrija PBMC su izolirani iz krvi zdravog davatelja i stimulirani s ISAC-om, mješavinom antitijela i adjuvansa, ili bez stimulusa 5-15 minuta na 37 stupnjeva. Nakon stimulacije, stanicefiksirani su dodavanjem 16 posto PFA (Electron microscopy sciences) do konačne koncentracije od 1,6 posto i inkubirani 1 0 minuta na sobnoj temperaturi (RT). Fiksirane stanice isprane su medijem za bojenje stanica (CSM; PBS s 0.5 posto BSA i 0,02 posto natrijevog azida (sve Sigma) i barkodirane pristupom koji se temelji na paladiju kao što je prethodno opisano 54. Uzorci s barkodom spojeni su u jedan kompozitni uzorak za površinsko bojenje.
Površinsko bojenje provedeno je dodavanjem protutijela (dodatna tablica 2) u CSM i inkubacijom 3{{10}} minute na sobnoj temperaturi. Anti-ljudska antitijela su kupljena konjugirana (Fluidigm) ili konjugirana na izotope teških metala pomoću MaxPar X8 pribora za označavanje antitijela (Fluidigm) prema preporukama proizvođača. Površinski obojene stanice isprane su jednom u CSM i permeabilizirane s MeOH 10 minuta na ledu. Permeabilizirane stanice isprane su dva puta s CSM i dodana su antitijela protiv intracelularnih antigena 30 minuta na sobnoj temperaturi. Stanice su isprane s CSM-om i konačno resuspendirane u interkalacijskoj otopini (1,6 posto PFA u PBS-u, 0,02 posto saponina (Sigma) i 0,5 μM iridijevog interkalatora (Fluidigm)) preko noći na 4 stupnja. Prije prikupljanja podataka uzorci su isprani jednom u CSM i dva puta u ddH2O. Svi uzorci su filtrirani kroz stanično cjedilo (Falcon) i resuspendirani na 1x106 stanica/mL u ddH2O dopunjenom s 1x EQ četveroelementnim kalibracijskim zrncima (Fluidigm), a podaci su prikupljeni na CyTOF2 masenom citometru (Fluidigm). Signalni odgovori procijenjeni su pomoću implementacije SPADE unutar Citibank 29. Analize su provedene na svim stanicama (bez smanjenja uzorkovanja), odabirom navedenog broja klastera i korištenjem svih relevantnih površinskih markera, ali ne i unutarstaničnih markera za klasteriranje. Linije imunoloških stanica označene su na temelju njihovih visokodimenzionalnih uzoraka površinske ekspresije proteina. Statističke analize provedene su u R, okruženju statističkog softvera otvorenog koda. Unutar svake podskupe stanica, terapijske skupine i donora izračunata je prosječna promjena puta za sljedećih dvadeset fosfoproteinskih markera: p-Src, p-STAT5, p-cMET, p-AKT, p-MAPKAPK2, p-SHP2, p -SLP76, p-IRF-7, p-ZAP70/SYK, p-CREB, p-NFKB, p-PI3K, IKB (ukupno), p-PLCG1, p-ERK1/2, p-p38, p -BTK/ITK, p-S6, p-STAT3 i p-JNK/SAPK. Prosječna promjena puta ponderirana je ukupnim brojem stanica u svakom klasteru, kako je definirano nakon SPADE klasteriranja. Provedeni su upareni t-testovi kako bi se procijenila razlika u prosječnoj promjeni nabora i testirala nulta hipoteza da nije bilo razlike u promjeni prosječnog nabora svakog markera u različitim uvjetima liječenja i kontrole.

Eksperimentalni postupak modela ksenotransplantata tumora Stanične linije tumora kupljene su od ATCC (NCI-N87, HCC1954 i COLO205) ili AddexBio (JIMT-1) i uzgajane u skladu sa smjernicama proizvođača. Stanice su sakupljene kada su dosegle 80-90 posto konfluentnosti odvajanjem s Accutase (Stemcell), isprane s PBS-om, resuspendirane na 40 x 106 stanica/mL u PBS-u i stavljene na led ne duže od dva sata. Neposredno prije implantacije, suspendirane stanice pomiješane su s jednakim volumenom Cultrex PathClear BME, tip 3 (R&D Systems) i 100 μL smjese (2 x 106 stanica) implantirano je supkutano u desni bok 6-8-tjedna -stare ženke miševa kako slijedi: NCI-N87 i COLO205 stanice implantirane su u NSG miševe (Jackson Laboratory), HCC1954 i JIMT-1 stanice implantirane su u Rag2/IL2rg dvostruko nokautiran (Taconic) i HCC1954 (za procjenu s T785-ISAC) su implantirani u NSG iliSCID/bež miševi (Jackson Laboratory ili Taconic i Envigo). Veličina tumora je bilježena dva puta tjedno i procijenjena je pomoću sljedeće formule: (duljina x širina2)/2. Nakon što su tumori dosegli 50-100 mm3, obično u roku od tjedan dana od implantacije tumora, započeto je liječenje. Miševi su randomizirani prema veličini tumora u skupine za liječenje prije početnog liječenja. Trastuzumab (EirGenix; EG12014), Trastuzumab ISAC ili Isotype ISAC pripremljen je u PBS-u od 1 mg/mL i primijenjen u dozi od 5 mg/kg intraperitonealno svakih pet dana (Q5D) za ukupno šest doza. Miševi čiji tumori prelaze 2000 mm3 su eutanazirani.
Eksperimentalni postupak stanične deplecije HCC1954 i MMC-a Kako bi se iscrpili makrofagi i druge fagocitne stanice, miševi koji su nosili HCC1954 ili MMC tumore liječeni su intraperitonealnom injekcijom dva dana prije početnog ISAC tretmana liposomima klodronata ili kontrolnim liposomima koji ne sadrže klodronat kao negativnu kontrolu (Encapsula, katalog # CLD-8901) i zatim liječen dva puta tjedno ukupno tri tjedna. Da bi se smanjili neutrofili, miševi su tretirani deplecijskim antitijelima 1A8 da bi se smanjili samo Ly6G plus neutrofili (BioXCell katalog # BE0075-1) ili RB6-8C5 da bi se smanjili Gr1 plus stanice, što uključuje Ly6G plus neutrofile i Ly6C plus stanice (BioXCell katalog # BE0075) ili izotipske kontrole 2A3 i LTF-2 (BioXCell katalog # BE0089 i BE0090, respektivno) dva dana prije početnog tretmana ISAC-om, zatim tretirani dva puta tjedno tijekom tri tjedna. Deplecija stanica u krvi potvrđena je protočnom citometrijom (dodatna slika 24). Postupak analize tumorskih citokina i mRNA Tumori su implantirani kao što je prethodno opisano i prikupljeni su za analizu u naznačenim vremenskim točkama nakon tretmana. Za imunohistokemiju i analizu mRNA, tumori su razdvojeni, a mRNA je analizirana NanoString panelom za profiliranje imunološkog profila miša pan-cancer. Analiza podataka provedena je softverom nSolver Advanced Analysis Software prema preporukama proizvođača. Dijagrami vulkana nacrtani su paketom ggplot2 u R. Da bi se dobili tumorski lizati za analizu citokina, fragmenti tumora su držani u prethodno napravljenom puferu (1 tableta inhibitora proteaze Pierce (Thermo Fisher, katalog #A32965) otopljena u 20 mL T- PER reagens za ekstrakciju proteina tkiva, Thermo Fisher, katalog #78510) u GentleMACS M epruvetama (Miltenyi, katalog #130-093-236) odmah nakon obdukcije. Uzorci tumora zatim su disocirani pomoću GentleMACS Octo Dissociatora. Svi su uzorci nakon toga centrifugirani 5 minuta na 300 g. Supernatanti su zatim sakupljeni u epruvete za mikrocentrifuge i ponovno centrifugirani. Analiza citokina provedena je na supernatantima pomoću MSD-a. Imunohistokemija je provedena korištenjem hematoksilina i eozina za identifikaciju strukture tkiva, kao i za sljedeće markere gdje su navedeni u studijama: CD11c (CST katalog #87585) i CD8 (CST katalog #98941).
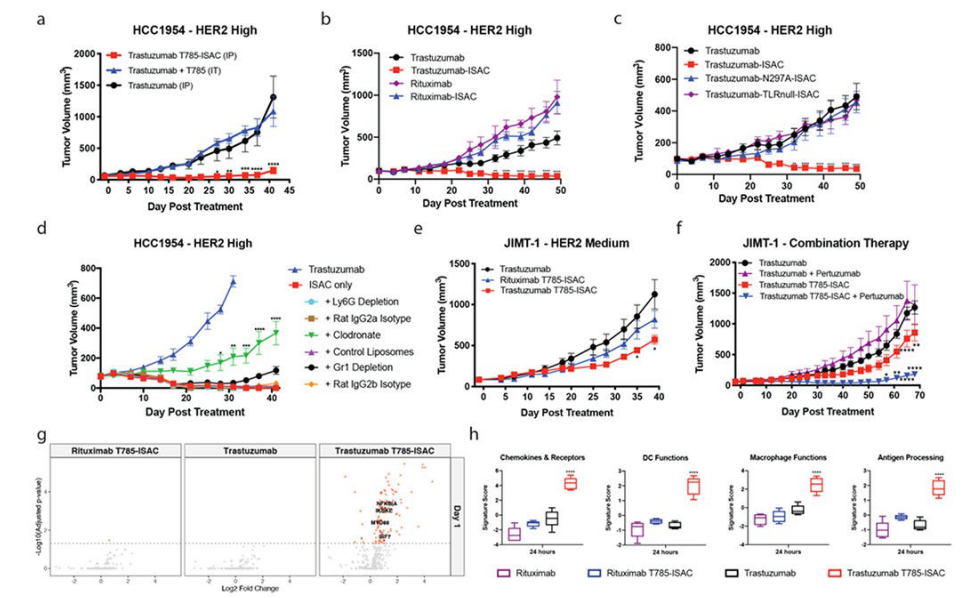

Slika 4: T785-ISAC izazivaju snažan antitumorski imunitet u modelima ksenografta tumora otpornih na trastuzumab. (ad) SCID/Beige ili NSG miševima implantirana je HCC1954 tumorska stanična linija i randomizirani su kada je volumen tumora dosegao 50 – 75 mm3. (a) Miševi su liječeni jednom intraperitonealno (IP) s 5 mg/kg trastuzumaba T785-ISAC ili trastuzumaba, ili s molarnim ekvivalentom doziranja mješavinom trastuzumaba i T785 u ISAC putem intratumorske (IT) injekcije. Podaci su iz jednog eksperimenta s n=3-5 miševa po skupini. (b) Miševi su liječeni intraperitonealnom injekcijom s 5 mg/kg trastuzumaba, trastuzumab-ISAC,rituksimab ili rituksimab-ISAC Q5DX6 (n= 5 miševa po skupini). (c) Miševi su liječeni intraperitonealnom injekcijom s 5 mg/kg trastuzumaba, trastuzumaba T785-ISAC, trastuzumaba N297A-ISAC ili trastuzumaba TLRnull-ISAC (n=5 miševa po skupini). (d) HCC1954 tumorske stanice implantirane su u SCID/Beige miševe, a stanice od interesa su iscrpljene prije i tijekom tretmana trastuzumabom T785-ISAC (5 mg/kg, Q5DX3) korištenjem anti-Ly6G antitijela (kontrola IgG2a štakora) , klodronat liposomi (kontrolni liposomi kao kontrola) ili anti-Gr1 antitijela (štakorski IgG2b kontrola). Podaci su iz jednog eksperimenta s n=4-6 miševa po skupini. (e, f) NSG ili Rag2/IL2rg dvostruki knockout miševi bili su implantirani s JIMT-1 staničnom linijom tumora i randomizirani kada je volumen tumora dosegao 50 – 75 mm3. Miševi su zatim tretirani naznačenim tretmanima od 5 mg/kg intraperitonealno s učestalošću (e) Q5DX6ili (f) Q5DX5 (n=3-6 miševa po skupini). (bf) Prikazani podaci reprezentativni su za najmanje dva eksperimenta. (gj) HCC-1954 tumori sakupljeni su iz kohorti miševa u naznačenim vremenskim točkama nakon tretmana s jednom dozom od 5 mg/kg ISAC ili kontrolnih antitijela. Tumori su obrađeni za analizu protočnom citometrijom, kvantifikaciju NanoString mRNA ili su fiksirani u formalinu i umetnuti u parafin za imunohistokemiju. (g) Dijagrami vulkana prikazuju log2 puta promjenu ekspresije gena u tretiranim u odnosu na izotipske kontrolne tumore mjerene NanoStringom nakon 24 sata (n=5 miševa po skupini). Promjene s prilagođenom p-vrijednošću od < 0.05="" prikazane="" su="" crvenom="" bojom.="" (h)="" rezultati="" genskog="" potpisa="" kvantificirani="" pomoću="" nsolver="" advanced="" analysis="" pathway="" score="" za="" tumore="" analizirane="" 24="" sata="" nakon="" tretmana="" (n="5" miševa="" po="" skupini).="" (i)="" analiza="" protočne="" citometrije="" tumorskog="" staničnog="" sastava="" 24="" sata="" i="" 7="" dana="" nakon="" tretmana="" (n="2-4" miševa="" po="" skupini).="" podaci="" su="" reprezentativni="" za="" najmanje="" 2="" eksperimenta.="" (j)="" reprezentativne="" slike="" kao="" i="" kvantifikacija="" f4/80="" i="" cd11c="" ihc="" tumora="" sakupljenih="" 9="" dana="" nakon="" svakog="" naznačenog="" tretmana.="" mjerne="" trake="" su="" 50="" μm.="" (aj)="" podaci="" su="" prikazani="" kao="" srednja="" vrijednost="" sa="" sem,="" a="" statistika="" je="" prikazana="" sa=""><0.05,><0.01,><0.001,><>
Eksperimentalni postupak modela singenog tumoraMMC stanice su dobivene od dr. Disisa (Sveučilište Washington) i uzgajane su u RPMI 1640 s dodatkom 20 posto FBS-a, 1 posto penicilin-streptomicina i L-glutamina na 37 stupnjeva i 5 posto CO2 do {{8 }} posto konfluentno. CT26 stanice (ATCC) transficirane da stabilno eksprimiraju HER2 protein štakora uzgajane su u RPMI 1640 dopunjenom s 10 posto FBS i 600 ug/mL G418 selektivnog antibiotika (Thermo) na 37 stupnjeva i 5 posto CO2 do 80-90 posto konfluenta. Nakon što su dovoljno konfluentne, stanice su sakupljene odvajanjem s Accutase (Stemcell) i ispiranjem s PBS. Sakupljene stanice resuspendirane su pri 20 x 106 stanica/mL (MMC)ili 5 x 106 stanica/mL (CT26-rHER2) u PBS-u i čuvati na 4 stupnja/na ledu do upotrebe. 100 μLsuspendiranih stanica supkutano su implantirane u 6-8- tjedan dana stare FVB/N-TgN(MMTV-Erbb2)NK1Mul/Jmiševe (MMC model, The Jackson Laboratory) ili ženke BALB/c miševa (CT26 model, The Jackson Laboratory) . Veličina tumora je mjerena i zabilježena dva putatjedan dana za vrijeme trajanja studija. Volumen tumora procijenjen je pomoću sljedeće formule: (duljina x širina2)/2. Nakon što su tumori dosegli 200-500 mm3 (MMC) ili 50-100 mm3 (CT26-rHER2), obično u roku od jednog tjedna od implantacije tumora, započeto je liječenje. Miševi su randomizirani prema veličini tumora u skupine za liječenje prije početkaliječenje. Anti-rHER2 mAb (BioXCell; 7.16.4) ili anti-rHER2-ISAC primijenjeni su intraperitonealno (učestalost kao što je naznačeno u legendama slika) tijekom trajanja studije.Miševi čiji tumori prelaze 2000 mm3 su eutanazirani. Procijenjeno je smanjenje T-stanicakod životinja koje koriste CD4 (BioXCell; GK1.5) ili CD8 (BioXCell; YTS 169.4) antitijela koja uništavaju stanice. Deplecija je započeta prije implantacije tumora i nastavljena primjenom 200 ug po protutijelu dvaput tjedno. Za ponovno izazivanje tumora, CT26 i 4T1 stanične linije su implantirane u 5 x 106 stanica po tumorskoj liniji, a miševi koji nisu imali tumor su izazivani s obje stanične linije kao kontrole.
Dodatni materijal Pogledajte web verziju na PubMed Central za dodatni materijal. Zahvale: Autori žele zahvaliti P. Basto, NE Reticker-Flynnu, T. Prestwoodu i B. Malletu na njihovoj korisnoj raspravi. Također zahvaljujemo Stanford Blood Center Flow Cytometry Core, posebno L. Tolentino, O. Choi i N.Wu. Također izražavamo našu zahvalnost dr. Mary L. (Nora) Disis i Denise Cecil sa Sveučilišta u Washingtonu koje su osigurale staničnu liniju MMC tumora.

Financiranje: SE Ackerman dobio je potporu stipendije Stanford BioX Bowes.
Literatura:1. Davis TA i sur. Terapija rituksimabom anti-CD20 monoklonskim protutijelima u ne-Hodgkinovom limfomu: sigurnost i učinkovitost ponovnog liječenja. J Clin Oncol 18, 3135-3143, doi:10.1200/JCO.2000.18.17.3135 (2000). [PubMed: 10963642]2. Grillo-Lopez AJ i sur. Rituximab: prvo monoklonsko protutijelo odobreno za liječenje limfoma. Curr Pharm Biotechnol 1, 1-9 (2000). [PubMed: 11467356]3. Lizotte PH i sur. Multiparametrijsko profiliranje karcinoma pluća nemalih stanica otkriva različite imunofenotipove. JCI Insight 1, e89014, doi:10.1172/jci.insight.89014 (2016). [PubMed: 27699239]4. Spranger S i sur. Gustoća imunogenih antigena ne objašnjava prisutnost ili odsutnost tumorskog mikrookruženja upaljenog T-stanicama u melanomu. Proc Natl Acad Sci USA 113, E7759-E7768, doi:10.1073/pnas.1609376113 (2016). [PubMed: 27837020] 5. Beatty GL & Gladney WL Mehanizmi imunološkog bijega kao vodič za imunoterapiju raka. Clin Cancer Res 21, 687–692, doi:10.1158/1078-0432.CCR-14-1860 (2015). [PubMed: 25501578]6. Fridman WH, Pages F, Salutes-Fridman C & Galon J Imunološki kontekst u ljudskim tumorima: utjecaj na klinički ishod. Nat Rev Cancer 12, 298–306, doi:10.1038/nrc3245 (2012). [PubMed: 22419253]
7. Galon J & Bruni D Pristupi liječenju imunoloških vrućih, promijenjenih i hladnih tumora s kombiniranim imunoterapijama. Nat Rev Drug Discov 18, 197–218, doi:10.1038/s41573-018-0007-y (2019). [PubMed: 30610226] 8. Gabrilovich DI, Ostrand-Rosenberg S & Bronte V Koordinirana regulacija mijeloidnih stanica tumorima. Nat Rev Immunol 12, 253-268, doi:10.1038/nri3175 (2012). [PubMed: 22437938]9. Joyce JA & Fearon DT Isključivanje T stanica, imunološka privilegija i tumorsko mikrookruženje. Znanost 348, 74–80, doi:10.1126/science.aaa6204 (2015). [PubMed: 25838376] 10. Carmi Y i sur. Akt i SHP-1 su DC-intrinzične kontrolne točke za imunitet tumora. JCI Insight 1, e89020, doi:10.1172/jci.insight.89020 (2016). [PubMed: 27812544]11. Carmi Y i sur. Alogeni IgG u kombinaciji s podražajima dendritičnih stanica inducira antitumorski T-stanični imunitet. Nature 521, 99-104, doi:10.1038/nature14424 (2015). [PubMed: 25924063]12. Allen BM i sur. Sistemska disfunkcija i plastičnost imunološkog mikrookruženja u modelima raka. Nat Med 26, 1125–1134, doi:10.1038/s41591-020-0892-6 (2020). [PubMed: 32451499]13. Sagiv-Barfi I i sur. Iskorenjivanje spontane malignosti lokalnom imunoterapijom. Sci Transl Med 10, doi:10.1126/scitranslmed.aan4488 (2018).14. Spitzer MH i sur. Za učinkovitu imunoterapiju raka potrebna je sustavna imunost. Cell 168, 487–502 e415, doi:10.1016/j.cell.2016.12.022 (2017). [PubMed: 28111070]15. Milhem Mohammed M., Theresa Medina RG, Kirkwood John M., Buchbinder Elizabeth, Mehmi Inderjit, Niu Jiaxin, Shaheen Montaser, Weight Ryan, Margolin Kim, Luke Jason, Morris Aaron, Mauro David, Krieg Arthur M., Ribas Antoni CT{ {77}}Intratumoralni agonist receptora sličnog naplati (TLR9), CMP-001, u kombinaciji s pembrolizumabom može poništiti otpornost na inhibiciju PD-1 u ispitivanju faze 1b kod ispitanika s uznapredovalim melanomom (AACR Annual Meeting 2018., 2018.).16. Rook AH Ljepota agonista TLR za CTCL. Blood 119, 321–322, doi:10.1182/ blood-2011-11-391243 (2012). [PubMed: 22247516]17. Singh M i sur. Učinkovita urođena i adaptivna imunost protiv melanoma putem lokalizirane aktivacije TLR7/8. J Immunol 193, 4722-4731, doi:10.4049/J Immunol.1401160 (2014). [PubMed:25252955]18. Zhao BG, Vasilakos JP, Tross D, Smirnov D & Klinman DM Kombinirana terapija koja cilja na toll-like receptore 7, 8 i 9 eliminira velike utvrđene tumore. J Immunother Cancer 2, 12, doi:10.1186/2051-1426-2-12 (2014). [PubMed: 24982761]19. Jurk M i sur. Ljudski TLR7 ili TLR8 neovisno daju odgovor na antivirusni spoj R-848. Nat Immunol 3, 499, doi:10.1038/ni0602-499 (2002). [PubMed: 12032557]20. Chattergoon MA i sur. HIV i HCV aktiviraju inflamasome u monocitima i makrofagima preko endosomalnih Toll-sličnih receptora bez indukcije interferona tipa 1. PLoS Pathog 10, e1004082, doi:10.1371/journal.bat.1004082 (2014). [PubMed: 24788318]21. Eigenbrod T, Pelka K, Latz E, Kreikemeyer B & Dalpke AH TLR8 osjeća bakterijsku RNA u ljudskim monocitima i igra neredundantnu ulogu za prepoznavanje Streptococcus pyogenes. J Immunol 195, 1092-1099, doi:10.4049/J Immunol.1403173 (2015). [PubMed: 26101323]22. Mattson G i sur. Praktičan pristup umrežavanju. Mol Biol Rep 17, 167-183 (1993). [PubMed: 8326953] 23. Gabay C, Ben-Bassat H, Schlesinger M & Laskov R. Somatske mutacije i intraklonalne varijacije u preuređenim Vkappa genima staničnih linija B-non-Hodgkinovog limfoma. Eur J Haematol 63, 180–191, doi:10.1111/j.1600-0609.1999.tb01766.x (1999). [PubMed: 10485273]24. Alonso MN i sur. Stanice T(H)1, T(H)2 i T(H)17 upućuju monocite da se diferenciraju u specijalizirane podskupove dendritičnih stanica. Blood 118, 3311–3320, doi:10.1182/blood-2011-03-341065 (2011). [PubMed: 21813450]25. Clarke SR i sur. Karakterizacija ovalbumin-specifične TCR transgene linije OT-I: MHC elementi za pozitivnu i negativnu selekciju. Immunol Cell Biol 78, 110-117, doi:10.1046/j.1440-1711.2000.00889.x (2000). [PubMed: 10762410]26. Zehn D, Lee SY & Bevan MJ Potpun, ali ograničen odgovor T-stanica na antigen vrlo niskog afiniteta. Nature 458, 211–214, doi:10.1038/nature07657 (2009). [PubMed: 19182777]27. Kondratova M i sur. Karta signalne mreže u više razmjera urođenog imunološkog odgovora kod raka otkriva potpise stanične heterogenosti. Nat Commun 10, 4808, doi:10.1038/s41467-019-12270-x (2019). [PubMed: 31641119]
28. Bendall SC i sur. Citometrija jednostanične mase diferencijalnog imunološkog odgovora i odgovora na lijekove u ljudskom hematopoetskom kontinuumu. Science 332, 687–696, doi:10.1126/science.1198704 (2011).[PubMed: 21551058]29. Qiu P i sur. Izdvajanje stanične hijerarhije iz visokodimenzionalnih citometrijskih podataka pomoću SPADE. Nat Biotechnol 29, 886-891, doi:10.1038/nbt.1991 (2011). [PubMed: 21964415]30. Kawai T & Akira S TLR signalizacija. Cell Death Differ 13, 816-825, doi:10.1038/sj.cdd.4401850 (2006). [PubMed: 16410796]31.Sanchez-Mejorada G & Rosales C Transdukcija signala imunoglobulinskim Fc receptorima. J Leukoc Biol 63, 521-533 (1998). [PubMed: 9581795] 32. Krishnaswamy S i sur. Sustavna biologija. Analiza signalizacije T stanica u podacima jedne stanice temeljena na uvjetnoj gustoći. Science 346, 1250689, doi:10.1126/science.1250689 (2014). [PubMed: 25342659]33. Kiefer F i sur. Syk protein tirozin kinaza bitna je za signalizaciju Fcgamma receptora u makrofagima i neutrofilima. Mol Cell Biol 18, 4209-4220 (1998). [PubMed: 9632805] 34. Braselmann S i sur. R406, oralno dostupan inhibitor tirozin kinaze slezene, blokira signalizaciju Fc receptora i smanjuje upalu posredovanu imunološkim kompleksom. J Pharmacol Exp Ther 319, 998-1008, doi:10.1124/jpet.106.109058 (2006). [PubMed: 16946104]35. Bruhns P i sur. Specifičnost i afinitet ljudskih Fcgamma receptora i njihovih polimorfnih varijanti za humane IgG podklase. Blood 113, 3716–3725, doi:10.1182/blood-2008-09-179754 (2009). [PubMed: 19018092]36. Nimmerjahn F & Ravetch JV Divergentna aktivnost podklase imunoglobulina g kroz selektivno vezanje Fc receptora. Znanost 310, 1510–1512, doi:10.1126/science.1118948 (2005). [PubMed: 16322460]37. Jefferis R Rekombinantna terapija antitijelima: utjecaj glikozilacije na mehanizme djelovanja. Trends Pharmacol Sci 30, 356-362, doi:10.1016/j.tips.2009.04.007 (2009). [PubMed: 19552968]38. Tanji H, Ohio U, Shibata T, Miyake K & Shimizu T. Strukturalna reorganizacija 8 dimera Toll-like receptora induciranih agonističkim ligandima. Science 339, 1426–1429, doi:10.1126/ science.1229159 (2013). [PubMed: 23520111]39. Shultz LD i sur. Razvoj ljudskih limfoidnih i mijeloidnih stanica kod NOD/LtSz-navedenih IL2R gama nultih miševa kojima su usađene mobilizirane ljudske hemopoetske matične stanice. J Immunol 174, 6477-6489, doi:10.4049/J Immunol.174.10.6477 (2005). [PubMed: 15879151]40. Xia Z i sur. Urođeni imunološki odgovor na implantaciju fibroblastičnih stanica ljudske koštane srži u CB17 SCID/bež miševa. J Cell Biochem 98, 966-980, doi:10.1002/jcb.20730 (2006). [PubMed: 16795075]41. Tanner M i sur. Karakterizacija nove stanične linije ustanovljene od pacijentice s rakom dojke otpornim na herceptin. Mol Cancer Ther 3, 1585-1592 (2004). [PubMed: 15634652]42. Luque-Cabal M, Garcia-Teijido P, Fernandez-Perez Y, Sanchez-Lorenzo L & Palacio-Vazquez I Mehanizmi koji stoje iza otpornosti na trastuzumab kod NJEZINOG2-pojačanog raka dojke i strategije za prevladavanje To. Clin Med Insights Oncol 10, 21-30, doi:10.4137/CMO.S34537 (2016). [PubMed: 27042153] 43. Li JY i sur. Biparatopni konjugat HER2-ciljanog antitijela i lijeka izaziva regresiju tumora u primarnim modelima otpornim na ili nepodobnim za ciljanu terapiju HER2-. Cancer Cell 29, 117–129, doi:10.1016/j.ccell.2015.12.008 (2016). [PubMed: 26766593]44. Ning S, Pagano JS & Barber GN IRF7: aktivacija, regulacija, modifikacija i funkcija. Genes Immun 12, 399–414, doi:10.1038/gene.2011.21 (2011). [PubMed: 21490621]45. Cao Q i sur. Bubrežni F4/80 plus CD11c plus mononuklearni fagociti pokazuju fenotipske i funkcionalne karakteristike makrofaga u zdravstvenoj i adriamicinskoj nefropatiji. J Am Soc Nephrol 26, 349-363, doi:10.1681/ASN.2013121336 (2015). [PubMed: 25012165] 46. Sheng J i sur. Diskretna podskupina stanica izvedenih iz monocita među tipičnim konvencionalnim dendritskim stanicama tipa 2 može se učinkovito unakrsno predstaviti. Cell Rep 21, 1203–1214, doi:10.1016/ j.celrep.2017.10.024 (2017). [PubMed: 29091760]
47. Knutson KL, Almand B, Dang Y & Disis ML Neu antigen-negativne varijante mogu se generirati nakon terapije neu-specifičnim antitijelima u neu transgenih miševa. Cancer Res 64, 1146-1151 (2004). [PubMed: 14871850] 48. Moynihan KD i sur. Iskorijenjivanje velikih ustanovljenih tumora kod miševa kombiniranom imunoterapijom koja uključuje urođene i adaptivne imunološke odgovore. Nat Med 22, 1402-1410, doi:10.1038/nm.4200 (2016). [PubMed: 27775706] 49. Siebenlist U, Franzoso G & Brown K Struktura, regulacija i funkcija NF-kappa B. Annu Rev Cell Biol 10, 405-455, doi:10.1146/annurev.cb.10.110194.002201 (1994.) . [PubMed: 7888182]

Slika 6: ISAC-ovi koji sadrže CL264- izazivaju uklanjanje tumora u HER2 mediju koji eksprimira ksenografte i uklanjanje tumora posredovano T stanicama, imunološku memoriju i širenje epitopa u modelu singenog tumora. (a) Kemijske strukture pomoćnih sredstava T785 i CL264 korištenih za stvaranje ISAC-a. (b) NSG miševi kojima je implantirana HCC1954 tumorska stanična linija randomizirani su kada je volumen tumora dosegao 50 – 75 mm3. Miševi su liječeni jednom intraperitonealnom injekcijom 5 mg/kg trastuzumaba, trastuzumaba T785-ISAC ili trastuzumaba CL264-ISAC. Tumori su sakupljeni 20 sati nakon primjene, obrađeni u suspenziju jedne stanice i analizirani protočnom citometrijom kako bi se procijenila aktivacija mijeloidnih APC-ova koji infiltriraju tumor. (cd) NSG ili Rag2/IL2rg dvostruki knockout miševi implantirani su s naznačenom staničnom linijom ljudskog tumora i randomizirani kada je volumen tumora dosegao 50 – 75 mm3 (HCC1954) ili 75 – 150 mm3 (JIMT-1). Miševi su liječeni intraperitonealnom injekcijom s 5 mg/kg rituksimaba, trastuzumaba, trastuzumaba T785-ISAC, trastuzumaba CL264-ISAC ili odgovarajućeg izotipa-ISAC, svakih 5 dana za ukupno 6 tretmana. (e) Ekspresija rHER2 mjerena je na CT26-rHER2 tumorskim stanicama u kulturi prije implantacije (lijevi dijagram protoka) i u tumorima devet dana nakon implantacije (desni grafikon protoka) protočnom citometrijom s fluorescentno konjugiranim anti-rHER2 protutijelima (crvena) ili kontrola izotipa (plava). (f) Balb/c miševima implantirana je CT26-rHER2 tumorska stanična linija i randomizirani su kada je volumen tumora dosegao 50mm3. Miševi su zatim liječeni intraperitonealnom injekcijom s 10 mg/kg mišjeg anti-štakorskog sredstvaHER2 ili mišji anti-štakorski HER2 CL264-ISAC svakih 5 dana za ukupno 6 tretmana. Prikazani podaci potječu iz 1 eksperimenta s 8 miševa po kraku i reprezentativni su za 3 eksperimenta.
(g) Anti-rat HER2 CL264-ISAC treated mice that experienced complete tumor regression for >21 dan nakon posljednjeg tretmana bili su izazvani roditeljskim staničnom linijom CT26 (lijevo krilo) i 4T1 (desno krilo), sa ili bez deplecije T stanica CD4 i CD8 (svaka po n =3). Miševi koji nisu imali tumor (n=6) inficirani roditeljskim staničnim linijama CT26 i 4T1 uključeni su kao kontrole. (ai) Podaci su prikazani iz pojedinačnih eksperimenata s 3-6 miševa po ruci i reprezentativni su za 1-4 pokuse s najmanje 3 miša po ruci u svakom eksperimentu. Podaci su prikazani kao srednja vrijednost sa SEM, a statistika je prikazana sa *P<><0.01,><0.001, and=""><>
50. Vogelpoel LT i sur. FcgammaRIIa unakrsna veza s TLR-ovima, IL-1R i IFNgammaR selektivno modulira proizvodnju citokina u ljudskim mijeloidnim stanicama. Imunobiologija 220, 193–199, doi:10.1016/j.imbio.2014.07.016 (2015). [PubMed: 25108563] 51. Daley JM, Thomas AA, Connolly MD, Reichner JS & Albina JE Upotreba Ly6G-specifičnog monoklonskog antitijela za depleciju neutrofila u miševa. J Leukoc Biol 83, 64–70, doi:10.1189/jlb.0407247 (2008). [PubMed: 17884993] 52. Broz ML i sur. Seciranje mijeloičnog odjeljka tumora otkriva rijetke aktivirajuće stanice koje predstavljaju antigen kritične za imunitet T stanica. Cancer Cell 26, 938, doi:10.1016/ j.ccell.2014.11.010 (2014).53. Spranger S, Dai D, Horton B & Gajewski TF Batf3 dendritičke stanice koje borave na tumoru potrebne su za promet efektorskih T stanica i adoptivnu terapiju T stanicama. Cancer Cell 31, 711–723 e714, doi:10.1016/j.ccell.2017.04.003 (2017). [PubMed: 28486109] 54. Zunder ER i sur. Crtično kodiranje stanica temeljeno na paladiju sa shemom dvostrukog filtriranja i algoritmom dekonvolucije jedne ćelije. Nat Protoc 10, 316–333, doi:10.1038/nprot.2015.020 (2015). [PubMed: 25612231]
