Dihotomni odgovori na kroničnu fetalnu hipoksiju dovode do unaprijed određenog fenotipa starenja Ⅱ
Nov 29, 2023
Hipoksičan
Fetalni bubrezi
Prikaz dereguliranog profila ekspresije proteina Kako bi se razjasnili molekularni putovi koji leže u pozadini IUGR-a uzrokovanog hipoksijom, svježe izolirani bubrezi iz hipoksičnih ili normoksičnih fetusa E18.5 podvrgnuti su odozdo prema gore profiliranju proteoma korištenjem nano-LC sustava (Dionex UltiMate 3{{9). }}00 RSLC) u kombinaciji s masenim spektrometrom visoke rezolucije (Thermo QExactive). Analiza glavnih komponenti pokazala je upečatljive razlike između hipoksičnih i normoksičnih bubrega (slika 2A). Ukupno je identificirano 6307 proteina (FDR <0,01, dodatna tablica S2) od kojih je 436 bilo značajno deregulirano (FDR <0,05); 284 s povećanom brojnošću i 152 s smanjenom brojnošću. Grupiranje funkcionalnih napomena korištenjem genske ontologije (18-20) otkrilo je obogaćivanje specifičnih mitohondrijskih, lizosomalnih, RNA- i DNA-vezujućih proteina, kao i proteina uključenih u specifične metaboličke procese ili urođene imunološke odgovore (Slika 2, B-D) . Te smo proteine kategorizirali s obzirom na (1) stvaranje nefrona, (2) metaboličku prilagodbu i (3) ubrzano starenje, kao što je predstavljeno i raspravljeno u sljedećim odlomcima.

Potisnuta replikacija DNA i sinteza proteina pridonose ograničenom stvaranju novih nefrona u kroničnoj hipoksiji
Štetni događaji tijekom razvoja, poput kronične fetalne hipoksije, često su se pokazivali povezani sa smanjenim brojem nefrona (27, 29-32). Ipak, temeljni mehanizam koji uvjerljivo objašnjava ovo otkriće rijetko se može dokazati. Grupiranje svih 64 dereguliranih proteina koji pripadaju GO-terminima "DNA-vezivanje" i "RNA-vezivanje" (toplinska karta je prikazana na dodatnoj slici S2) pomoću baze podataka STRING (22) otkrilo je više podmreža uključujući popravak DNA, replikaciju DNA, spajanje mRNA i ribosomski proteini (slika 3A). Sveobuhvatniji popis obogaćenih procesa ili putova prikazan je na slici 3B (FDR < 0.05). Od ovih "Ribosom" i "DNA replikacija" bili su među glavnim terminima potisnutih proteina, dok su spajanje mRNA i "Razgradnja RNK" bili među glavnim terminima induciranih proteina. Procesi popravka DNK pokazali su bipartitni obrazac ekspresije. Ovdje su proteini uključeni u eksciziju nukleotida ili popravak neslaganja bili potisnuti, ali su inducirani oni koji posreduju u "popravku ekscizije baze". Nadalje, razina zastupljenosti inhibitora staničnog ciklusa p27Kip1 bila je dvostruko povećana (Slika 3C), a ona markera proliferacije Ki67 bila je 3{18}}puta smanjena (Slika 3D), što zajedno ukazuje na usporavanje stanice proces podjele. Konkretno, razina ekspresije mRNA Mki67, gena koji kodira za Ki67, bila je značajno potisnuta u mišjim primarnim proksimalnim tubularnim stanicama uzgojenim u uvjetima hipoksije (slika 3E). Ova represija je bila posredovana preko hipermetilacije Mki67 promotorske regije u hipoksičnim fetalnim bubrezima (slika 3F). Stoga, u fetalnim hipoksičnim bubrezima, čini se da su sinteza DNA, translacija mRNA i većina procesa popravka DNA smanjeni, smanjujući sposobnost stanica da rastu i proliferiraju. Ukupno gledano, po prvi put podaci profiliranja proteoma daju molekularne dokaze koji potencijalno objašnjavaju smanjeno stvaranje nefrona.
Urođeni imunološki sustav i oksidativni stres aktiviraju se u stanjima kronične hipoksije

Jedan od najobogaćenijih pojmova koji se pojavljuje u analizi funkcionalnih komentara svih 436 proteina i najviši za inducirane proteine bio je "degranulacija neutrofila" (Sl. 2, B i C), što ukazuje na aktivaciju urođenog imunološkog sustava u tijeku.hipoksični fetalni bubrezi. Od 34 povezana proteina, 29 je inducirano, a pet potisnuto (ružičasto na slici 4A). Među induciranim proteinima bilo je mnogo glikolitičkih enzima i enzima povezanih s lizosomima, nekoliko članova obitelji proteina S100A, inhibicijski faktor migracije upalnih citokina makrofaga (MIF), kao i proteini primarnih i sekundarnih zrnaca, protein neutrofilnih zrnaca (NGP), mijeloperoksidaza (MPO) , katelicidin (CAMP), protein za prepoznavanje peptidoglikana 1 (PGLYRP1) i laktoferin (LTF). Kako bi se potvrdila očekivana invazija neutrofila u bubrege hipoksičnog fetusa i kako bi se otkrila njihova lokacija unutar tkiva, bubrežni dijelovi su obojeni na MPO. MPO-pozitivne stanice formirale su nakupine u nefrogenoj zoni bubrežnog korteksa, u blizini krvnih žila, uz proksimalni tubul, a povremeno se mogu naći u medularnim regijama hipoksičnih uzoraka (Slika 4D i dodatna Slika S3, A –C). Nasuprot tome, normoksični fetalni bubrezi nisu pokazali infiltraciju ili nakupljanje neutrofila (slika 4C). Pokazalo se da Caveolin-1 (CAV1) pospješuje transcelularnu migraciju imunoloških stanica (33). Sukladno tome, CAV1 je induciran u hipoksičnim fetalnim bubrezima (dodatna slika S3D), pokazujući pojačano bojenje bubrežnih krvnih žila uključujući one koje prolaze kortikalnom regijom fetalnog bubrega (Slika 4, E i F). Degranulacija neutrofila dovodi do lokalnog izbijanja reaktivnih kisikovih vrsta što dovodi do povećanog oksidativnog stresa i oštećenja tkiva uključujući oksidaciju DNA. Važan marker oksidacije DNA je 8-hidroksi-2′ -deoksigvanozin (8-OHdG), koji je pojačan u proksimalnim tubulima i u nefrogenoj zoni hipoksičnih fetalnih bubrega (Slika 4, G i H), u blizini grupiranja neutrofila. Ovaj porast 8-OHdG oštećene DNK dogodio se unatoč istovremenoj indukciji MGMT i OGG1 (Slika 4, I i J), dva enzima odgovorna za uklanjanje 8-OHdG. Ovi rezultati pokazuju kontinuiranu aktivaciju prirodnog imunološkog sustava u bubregu u razvoju, što uzrokuje još više oštećenja tkiva uz hipoksični stres. Zajedno s neučinkovitim popravkom ovih lezija tkiva, može se pokrenuti začarani krug koji dodatno oštećuje nefrogenezu.

SLIKA 2. Proteomsko profiliranje otkriva višestruke promjene povezane s hipoksijom. A, analiza glavnih komponenti proteomskih podataka pokazala je jasnu razliku između normoksičnih i hipoksičnih fetalnih bubrega. B–D, grupiranje funkcionalnih napomena svih značajno dereguliranih proteina (B), induciranih proteina (C) i smanjenih proteina (D) Značajno promijenjeni udio puta (x-os) ucrtan je u odnosu na njegov značaj obogaćivanja (y- os). Veličina svake točke kodira ukupan broj članova na tom putu. Inducirani proteini pokazali su obogaćivanje metaboličkih procesa (glikoliza), mitohondrijskih ili lizosomalnih proteina i proteina uključenih u odgovor imunološkog sustava (degranulacija neutrofila), dok su reducirani proteini obogaćeni za puteve vezanja DNA i RNA (strukturni sastojak ribosoma).

(PGLYRP1) i laktoferina (LTF). Kako bi se potvrdila očekivana invazija neutrofila u bubrege hipoksičnog fetusa i kako bi se otkrila njihova lokacija unutar tkiva, bubrežni dijelovi su obojeni na MPO. MPO-pozitivne stanice formirale su nakupine u nefrogenoj zoni bubrežnog korteksa, u blizini krvnih žila, uz proksimalni tubul, a povremeno se mogu naći u medularnim regijama hipoksičnih uzoraka (Slika 4D i dodatna Slika S3, A –C). Nasuprot tome, normoksični fetalni bubrezi nisu pokazali infiltraciju ili nakupljanje neutrofila (slika 4C). Pokazalo se da Caveolin-1 (CAV1) pospješuje transcelularnu migraciju imunoloških stanica (33). Sukladno tome, CAV1 je induciran u hipoksičnim fetalnim bubrezima (dodatna slika S3D), pokazujući pojačano bojenje bubrežnih krvnih žila uključujući one koje prolaze kortikalnom regijom fetalnog bubrega (Slika 4, E i F). Degranulacija neutrofila dovodi do lokalnog izbijanja reaktivnih kisikovih vrsta što dovodi do povećanog oksidativnog stresa i oštećenja tkiva uključujući oksidaciju DNA. Važan marker oksidacije DNA je 8-hidroksi-2′ -deoksigvanozin (8-OHdG), koji je pojačan u proksimalnim tubulima i u nefrogenoj zoni hipoksičnih fetalnih bubrega (Slika 4, G i H), u blizini grupiranja neutrofila. Ovaj porast 8-OHdG oštećene DNK dogodio se unatoč istovremenoj indukciji MGMT i OGG1 (Slika 4, I i J), dva enzima odgovorna za uklanjanje 8-OHdG. Ovi rezultati pokazuju kontinuiranu aktivaciju prirodnog imunološkog sustava u bubregu u razvoju, što uzrokuje još više oštećenja tkiva uz hipoksični stres. Zajedno s neučinkovitim popravkom ovih lezija tkiva, može se pokrenuti začarani krug koji dodatno oštećuje nefrogenezu.
Metaboličke prilagodbe na hipoksiju rezultiraju izraženom glikolizom u fetalnom bubregu
Kronična hipoksija je teško stanje na koje se stanice moraju prilagoditi putem metaboličkih promjena kako bi preživjele. Najvažnije u tome je održavanje stanične proizvodnje ATP-a koja u nedostatku dovoljne oksigenacije zahtijeva prijelaz s oksidativne fosforilacije na glikolizu. Od svih izraza proizašlih iz funkcionalne anotacije, "glikolitički proces" bio je najznačajniji (slika 2B). Svih deset enzima (crveno ①–⑩ na slici 5A) potrebnih za pretvorbu glukoze u piruvat inducirano je ufetalni hipoksični bubreziu usporedbi s normoksičnim kontrolama (toplinska karta prikazana je na slici 5C). Nadalje, ekspresija transportera glukoze 1 (SLC2A1, narančasta na slici 4A) i laktat dehidrogenaze A (LDHA, tamnocrvena na slici 5A) također je pojačana, što bi trebalo olakšati povećani unos glukoze u stanicu i povećano smanjenje piruvata u laktat, redom. Čini se da je alternativna upotreba piruvata u ciklusu limunske kiseline onemogućena (1) pojačanom ekspresijom piruvat dehidrogenaze kinaze 1 (PDK1, tamnocrvena na slici 5A), koja inaktivira kompleks piruvat dehidrogenaze u mitohondrijima, a time i oksidaciju piruvata na acetil-CoA; i (2) smanjenim razinama piruvat karboksilaze (PC), koja katalizira pretvorbu piruvata u oksaloacetat. S druge strane, fruktoza-1,6-bisfosfataza 1 (FBP1, plavo na slici 5A) je smanjena, dodatno povećavajući potencijalni tok glukoze prema piruvatu. Sve te enzimske promjene pogoduju proizvodnji laktata, i doista, koncentracija laktata je povećana u hipoksičnim fetalnim bubrezima (Slika 5B). Povećana proizvodnja laktata može dovesti do nepovoljnog zakiseljavanja. Ipak, pronašli smo među obogaćenim proteinima monokarboksilatne transportere SLC16A3 i SLC5A8 (narančasti na slici 5A), za koje je poznato da izlučuju laktat u izvanstanični prostor kako bi izbjegli toksične učinke zakiseljavanja citoplazme. Dakle, naš model pokazuje izvanrednu sposobnost fetalnih bubrega da se prilagode kroničnoj hipoksiji povećanjem glikolitičke aktivnosti,

SLIKA 3. Stvaranje novih nefrona u hipoksiji povezano je s potisnutom replikacijom DNA i sintezom proteina. Mreža proteinske interakcije značajno promijenjenih proteina koji vežu DNA i RNA izvedena iz baze podataka STRING pokazuje nekoliko klastera proteina: ribosomske proteine (plavo), proteine uključene u replikaciju DNA (zeleno), popravak DNA (ljubičasto) i spajanje mRNA ( Crvena). Marker proliferacije Ki67 (Mki67) označen je crnom bojom, naglašavajući njegovu blisku povezanost s popravkom DNK i replikacijom DNK. B, izbor puteva značajno promijenjenih DNA- i RNA-vezujućih proteina iz baza podataka KEGG i Reactome koji su pokazali najistaknutije promjene uhipoksični bubrezi, prikazano u opadajućem redoslijedu od značaja. Procesi spajanja RNA i razgradnje RNA bili su obogaćeni (crveno), dok su putovi translacije RNA, replikacije DNA i popravka bili potisnuti (plavo). Samo procesi s FDR-om<0.05 are shown. C and D, the cell cycle inhibitor p27Kip1 was enhanced (unpaired two-tailed t test, Welch's correction, p = 0.0095), whereas the expression of the proliferation marker Ki67 was reduced (unpaired two-tailed t test, Welch's correction, p = 0.0078) in hypoxic fetal kidneys. E, hypoxia reduced the mRNA expression level of Mki67 in mouse primary proximal tubular cells (unpaired two-tailed t test, p < 0.0001). F, this reduction was mediated by hypermethylation of the Mki67 promoter in hypoxic fetal kidneys. Open circle unmethylated, black circle methylated (Fisher's exact test, p = 0.0016; Mann–Whitney U-test, p = 0.0431)
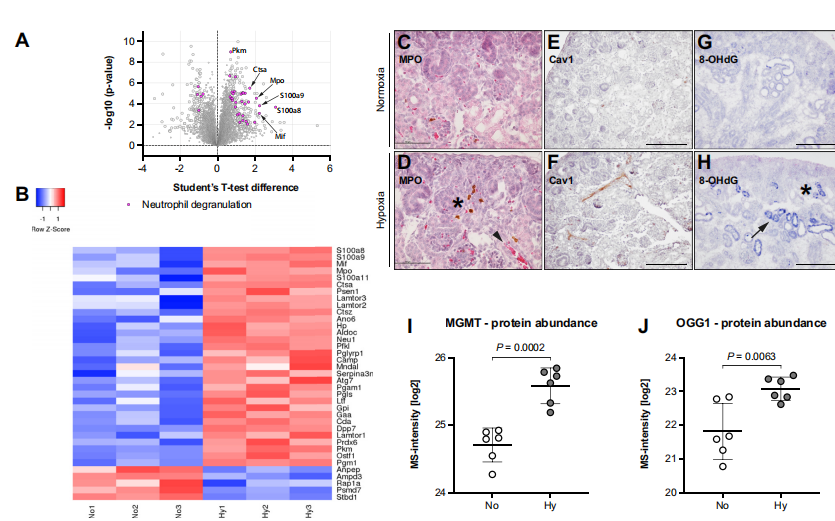
SLIKA 4. Proteini uključeni u upalni odgovor i oksidativni stres obogaćuju se u novonastalim nefronima pod hipoksijom. A, prikaz svih 34 značajno promijenjena proteina za napomenu nazvanu degranulacija neutrofila (ružičasti kružići) među svim značajnim (veći sivi kružići) i neznačajnim (manji sivi kružići) proteinima našeg skupa podataka. 29 imalo je višu razinu brojnosti, dok je pet bilo smanjeno. B, toplinska karta koja prikazuje sve ružičaste proteine u (A) i njihovu indukciju ili potiskivanje u hipoksiji, prikazane opadajućim redoslijedom obilja proteina. C–H, reprezentativne imunohistokemijske slike E18.5 normoksičnog ilihipoksični bubrezipokazujući infiltraciju neutrofila i oksidativni stres. C i D, imunohistokemija za neutrofilni marker mijeloperoksidazu (MPO) otkrila je grupiranje ovih stanica u blizini novonastalih nefrona (zvjezdica) i uz bubrežne krvne žile (strelica) hipoksičnih fetalnih bubrega (D). U normoksičnim kontrolama (C), MPO-pozitivne stanice bile su rijetko prisutne. (Skale 100 μm). E i F, imunohistokemija koja prikazuje pojačanu ekspresiju kaveolina-1 (CAV1) u bubrežnim krvnim žilama hipoksičnih fetalnih bubrega (F) u usporedbi s kontrolama (E) (ljestvice 200 μm). G i H, 8-hidroksi-2′ -deoksigvanozin (8-OHdG), marker za oksidativno oštećenje DNK, bio je značajno pojačan u novonastalim nefronima (zvjezdica) u bubrežnom korteksu i u stanice proksimalnih tubula (strelica) hipoksičnih bubrega (H), dok je samo nekoliko stanica obojeno u normoksičnom tkivu (G) (ljestvice 200 μm). I i J, ovo povećanje oštećenja DNK dogodilo se unatoč istovremenom porastu O-6-metilgvanin-DNK metiltransferaze (MGMT; nespareni dvostrani t test, p=0.0002) (I) i {{ 15}}okso gvanin glikozilaza (OGG1; nespareni dvostrani t-test, p=0.0063) (J), dva enzima uključena u popravak oksidirane DNA.

koji osigurava dovoljnu proizvodnju ATP-a i preživljavanje u ovim nepovoljnim uvjetima.
Fetalna hipoksija potiče kompenzacijski uvoz mitohondrijskih proteina i sklapanje dišnog lanca
Osim pojačane glikolize, pronašli smo višestruke promjene u razinama obilja mitohondrijskih proteina (toplinska karta prikazana je na dodatnoj slici S4). Generiranje proteinskih mreža korištenjem STRING otkrilo je nekoliko klastera koji sadrže proteine uključene u translokaciju proteina u mitohondrije, oksidativnu fosforilaciju i mitohondrijske ribosomske proteine (Slika 5, D i E). Treba napomenuti da je inducirano više proteina povezanih s unutarnjom mitohondrijskom membranom, mjestom gdje se odvija oksidativna fosforilacija (OXPHOS). OXPHOS obuhvaća pet multiproteinskih kompleksa raspoređenih duž unutarnje mitohondrijske membrane. Među induciranim proteinima bile su komponente OXPHOSkompleksa (NDUSF6), III (UQCR10), IV (COX6B1, COXC i COX7A2) i V (ATP5J, MTATP8), ali i UQCC3 i SCO2, koji su potrebni za pravilno sastavljanje i funkcioniranje kompleksa, odnosno IV (Slika 5D i dodatna Slika S4). SDHC i SDHD, podjedinice kompleksa ll, također su bile pojačane (1.6- i 2.5-puta, respektivno), ali nisu dosegle statističku značajnost. Štoviše, nisu samo komponente respiratornog lanca obogaćene fetalomhipoksični bubrezi, ali i mnoštvo proteina koji posreduju u njihovom uvozu u mitohondrije. To je uključivalo članove translokaze vanjske membrane (TOM - TOMM22) i kompleksa translokaze unutarnje membrane TIM22 (TIMM22, TIMM9 i TIMM10 i povezanog kompleksa TIMM8-TIMM13- (Slika 5D i dodatna Slika . S4). Među 21 mitohondrijskom proteinu sa smanjenim obiljem bila su četiri mitohondrijska ribosomska proteina, kao i proteini uključeni u katabolizam aminokiselina, biosintezu vitamina ili beta-oksidaciju masnih kiselina (Slika 5, D i E, i dodatna Slika 5). S4). Ovi nalazi ukazuju na potencijalnu disfunkciju mitohondrija i očite napore da se regeneriraju oštećeni proteini (34), unatoč pojačanoj glikolizi i sveukupno smanjenoj sintezi proteina.
Lizosomska biogeneza i autofagija su poboljšane uHipoksični fetalni bubreziLizosom je bio druga organela za koju se čini da je obogaćena u uvjetima hipoksije. Međutim, u usporedbi s mitohondrijima, gdje je 36% proteina smanjeno, gotovo svi proteini povezani s lizosomima su regulirani na gore (Slika 6, A i B). Među njima je bilo devet lizosomalnih kiselih hidrolaza, koje predstavljaju gotovo 20% lizosomalnih kiselih hidrolaza označenih u KEGG putu za lizosome: četiri proteaze (CTSA, CTSF, CTSZ, TPP1), tri glikozidaze (GAA, NAGA, NEU1), lizosomska kisele fosfataze 2 (ACP2) i lizosomske kisele lipaze A (LIPA). Nadalje, pronašli smo dokaze za povećanu biogenezu lizosoma i srodnih organela. Tri od osam komponenti BLOC1 (biogeneza kompleksa organela povezanih s lizosomom 1) značajno su inducirane (Slika 6, C–E), kao i transporter H/Cl izmjene 5 (CLCN5), koji je ključni igrač u acidifikacija endosoma (slika 6F). Treba napomenuti da Snapin (BLOC1 podjedinica 7) također igra ulogu u zakiseljavanju lizosoma te u sazrijevanju i funkciji autofagosoma. Drugi inducirani proteini za koje se zna da igraju ulogu u autofagiji bili su Atg7 i Bnip3 (Slika 6, G i H). Još jedan uvjet za autofagijski tok je perinuklearno grupiranje lizosoma, posredovano lizosomskim kompleksom Ragulator (35, 36) i dvjema suprotnim obiteljima motornih proteina. Zapanjujuće je da su četiri od pet članova podjedinica skele regulatora (LAMTOR1, 2, 3 i 5) značajno inducirana (Sl. 6, A i B); LAMTOR4 je također bio 1.81-struko induciran, ali nije dosegao statistički značaj. Nadalje, kinezini, koji posreduju u kretanju organela prema van, pokazali su tendenciju potiskivanja, dok su članovi obitelji dineina koji olakšavaju kretanje prema unutra inducirani, iako nisu statistički značajni (dodatna slika S5). Zajedno, ovi nalazi pružaju snažne dokaze da je kućna funkcija lizosoma poboljšana ufetalni hipoksični bubrezi, potpuno kompatibilan s očekivanom potrebom za obnavljanjem oštećenih mitohondrija.
Preuranjen
Starenje prikazuje Janusove aspekte hipoksične prilagodbe Za razliku od kompenzacijskih mehanizama popravka i pomlađivanja, pronašli smo 15 dereguliranih proteina koji pripadaju GO terminu "starenje" (Slika 7A), predstavljajući treću kategoriju hipoksičnih prilagodbi: ubrzano starenje . Iako većina ovih proteina igra ulogu u jednom od gore opisanih procesa degranulacije neutrofila i lizosoma (MIF, MPO, PSEN1), mitohondrija (NDUFS6, FADS1, MTCO1, CYP27B1), glikolize (ALDOC) i popravka DNA (OGG1) ; za neke je opisano da izravno utječu na životni vijek miševa. Konkretno, obilje proteina i klotho i sirtuina 6 je smanjeno u E18.5 hipoksicifetalni bubrezi(Sl. 7, B i C). Sirtuin 6 je sveprisutno izražen enzim s aktivnošću proteinske deacetilaze i mono-ADP ribozil transferaze uključen u regulaciju nekoliko staničnih funkcija, uključujući upalu, glikolizu i popravak DNA. Njegov nokaut dovodi do ozbiljne progerije kod miševa sa smanjenim životnim vijekom od 1 do 3 mjeseca (37, 38). Bubreg je glavno mjesto sinteze kloto (tj. distalni zavojiti tubul—DCT doprinosi većini proteina uz dodatnu sintezu u proksimalnim zavojitim tubulima), gdje djeluje lokalno kao membranski vezana beta-glukuronidaza. Čini se da je smanjena zastupljenost klothoa specifičan proces budući da drugi proteini DCT-a, uključujući CALB1, nisu promijenjeni. Klotho se također izlučuje u cirkulaciju bilo cijepanjem izvanstaničnog dijela membranski vezanog oblika ili translacijom alternativne spojene varijante. Razina cirkulirajućeg klotha (sKL) opada s dobi (39, 40), što nas je potaknulo da procijenimo njegovu koncentraciju i onu sirtuina 6 u krvi trupa hipoksičnih ili normoksičnih E18.5 fetusa. Doista, koncentracije sKL i sirtuina 6 bile su značajno smanjene u hipoksičnim E18.5 fetusima (Slika 7, D i E). Nadalje i važno, serumske razine klotha i sirtuina 6 također su bile značajno smanjene kod starih miševa (Slika 7, F i G), što ukazuje na trajno smanjenje ova dva proteina tijekom života. Za Klothoa, čini se da je to posljedica značajno smanjene razine ekspresije mRNA u bubrezima 15-mjesečnih hipoksičnih potomaka (Slika 7H). Međutim, razine bubrežne mRNA ekspresije sirtuina 6 bile su nepromijenjene između starih normoksičnih i hipoksičnih miševa (slika 7I). Nadalje, pokazalo se da su promjene u metilaciji DNA jedan od najvažnijih mehanizama ne samo za obnovu i diferencijaciju nefronskih progenitorskih stanica (41), već i za ekspresiju klotho (42, 43). Međutim, za razliku od hipermetilacije Mki67 (Sl. 3F), klotho promotor je bio hipometiliran tijekom kronične hipoksije (dodatna Slika S6). Uzorak metilacije Sirt6 nije se mogao odrediti. Koliko znamo, naš IUGR model je prvi koji ocrtava mehanizam koji dovodi do fenotipa preranog starenja, kroz sinergiju upalnog oštećenja, neučinkovitog oporavka, promijenjenog metabolizma i smanjene količine proteina protiv starenja koji se događaju već pri rođenju.
Smanjenje proteina protiv starenja kao odgovor na kroničnu hipoksiju postoji kod miševa i ljudi U posljednjem nizu eksperimenata, pitali smo je li međudjelovanje između kronične hipoksije i smanjenih razina proteina protiv starenja u serumu evolucijski očuvan fenomen. U tu svrhu, uzorci seruma iz kontrolirane studije (10) od devet zdravih dobrovoljaca (osam muškaraca, jedna žena) prikupljeni su 2 tjedna prije (razina mora, SL), u tri vremenske točke tijekom neprekinutog 28-dana boravak na 3454 m (visoka nadmorska visina, HA3, HA9, HA28), te 1, 7 i 14 dana nakon povratka u SL (RSL1, RSL7, RSL14) analizirani su za sKL i SIRT6 (slika 8). Uzorci dobiveni na SL služili su kao kontrola za svakog sudionika. Razine sKL i SIRT6 u serumu pale su na velikim nadmorskim visinama i obje su postigle statističku relevantnost na H28. Nakon povratka na razinu mora, sKL se povećao na razine više nego prije boravka na velikoj nadmorskoj visini na RSL7 i vratio se u normalu na RSL14 (Slika 8A). S druge strane, SIRT6 je nastavio opadati nakon povratka na razinu mora i tek se ponovno počeo naginjati na RSL14 (Slika 8B), što ukazuje na različitu regulaciju ova dva proteina protiv starenja. Ukratko, ovi nalazi sugeriraju da smanjene razine klotha i sirtuina 6 u serumu mogu općenito zahtijevati izlaganje kroničnim hipoksičnim stanjima i stoga mogu predstavljati evolucijski visoko očuvan proces.
Usluga podrške Wecistanche-najvećeg izvoznika cistanche u Kini:
E-pošta:wallence.suen@wecistanche.com
Whatsapp/telefon:+86 15292862950
Kupite za više pojedinosti o specifikacijama:
https://www.xjcistanche.com/cistanche-shop






