Schlafens može uspavati viruse, 2. dio
Jun 25, 2023
5. SLFN5 kao urođeni modulator imunološkog signala
Iako IFN-ovi tipa I igraju važnu ulogu u obrani domaćina od infekcije patogenom, njihova proizvodnja mora biti pravilno regulirana kako bi se izbjegle pretjerano štetne imunološke reakcije. Stoga su negativni regulatori neophodni za oporavak stanica od IFN signalizacije, budući da disregulacija proizvodnje IFN dovodi do autoimunih poremećaja. Neki ISG mogu regulirati putove koji utječu na njihovu ekspresiju, bilo pozitivno ili negativno.
Na primjer, ISG56 je povezan s adapterskim proteinom STING i prekida STING interakciju s nizvodnim molekulama VISA/MAVS ili TBK1, inhibirajući virusom induciranu aktivaciju IRF3, ekspresiju IFN-a i stanične antivirusne odgovore. Drugi negativni regulator je ISG15 dekonjugirajuća proteaza ubikvitin-specifična peptidaza 18 (USP18). USP18 inhibira JAK-STAT signalizaciju interakcijom s IFNAR2 na način neovisan o proteazi [64].
Razdvojna proteaza (uPA) je važna proteaza koja može razgraditi proteine u izvanstaničnom matriksu i sudjelovati u fiziološkim i patološkim procesima kao što su migracija stanica, metastaze tumora i angiogeneza. S druge strane, imunitet je važan obrambeni mehanizam ljudskog organizma od patogena i tumorskih stanica. Dakle, kakav je odnos između uPA i imuniteta?
Nekoliko je studija pokazalo da uPA može utjecati na funkciju imunološkog sustava kroz nekoliko mehanizama. Prvo, ekspresija uPA i njegovog receptora uPAR može regulirati migraciju i infiltraciju imunoloških stanica, čime utječe na pojavu upale i imunološkog odgovora. Drugo, uPA može aktivirati druge proteaze na površini imunoloških stanica, kao što su MMP, katepsini, itd., čime sudjeluje u biološkim procesima kao što su prijenos signala, proliferacija i diferencijacija. Ono što je najvažnije, uPA također može utjecati na proces imunološkog nadzora tumora, čineći ljudski imunološki sustav nesposobnim prepoznati i napasti stanice raka, čime se potiče rast tumora i metastaze.
Općenito, uloga uPA u rastu tumora i patologiji opsežno je proučavana, dok se njegov učinak na imunološki sustav tek treba dodatno istražiti. Buduća istraživanja mogu započeti od aspekata uPA u infiltraciji imunoloških stanica, imunološkoj regulaciji i imunološkom bijegu tumora, istražiti odnos između uPA i imunološkog sustava i dati nove ideje i ciljeve za razvoj liječenja tumora i imunoterapije. S tog gledišta moramo obratiti pozornost na poboljšanje našeg imuniteta. Cistanche može značajno poboljšati imunitet. Mesna pasta je bogata raznim antioksidativnim tvarima, poput vitamina C, vitamina C, karotenoida itd. Ovi sastojci mogu hvatati slobodne radikale i smanjiti oksidativni stres. Potiču i poboljšavaju otpornost imunološkog sustava.

Click cistanche tubulosa prednosti
Zabilježeno je da je ljudski SLFN5 negativni regulator transkripcije gena izazvane IFN-om [65]. Utvrđeno je da je STAT1 prisutan kao kompleks koji veže protein SLFN5 na način ovisan o IFN-u tipa I i veže se na ISRE element u promotoru ISG-ova. Čini se da SLFN5 služi kao represor STAT1-inducirane transkripcije gena kroz izravnu interakciju proteina. U skladu s ovim, pokazalo se da je SLFN5 obogaćen na promotorima tipa I IFN-inducibilnih ISG, gdje se STAT1 veže.
Eksperimenti s mikromrežama otkrili su da izbačene stanice SLFN5 izražavaju više ISG-a nego stanice divljeg tipa, što ukazuje na potencijalnu ulogu SLFN5 u regulaciji STAT1-posredovane transkripcijske aktivacije ISG-a izazvane IFN-om tipa I [65]. Slično, u ljudskim fibroblastima kožice i HeLa stanicama, bazalna razina ISG15, dobro poznatog antivirusnog proteina, povećana je zbog smanjenja SLFN5; dodatno, primijećena je brza indukcija ekspresije proteina ISG15 od strane DNA virusa, poput humanog citomegalovirusa (HCMV) [20]. Prema tome, čini se da je SLFN5 transkripcijski supresor transkripcije gena za IFN, kao i gen odgovora stimuliranog IFN-om.
ZEB proteini su transkripcijski faktori vezanja homeoboksa cinkovog prsta E najpoznatiji po svojoj ulozi u pokretanju tranzicije epitela u mezenhim i metastaza kod nekih vrsta raka, uključujući BRCA mutirane stanice raka [66,67]. Također ih široko izražavaju imunološke stanice i reguliraju važne transkripcijske mreže potrebne za diferencijaciju, održavanje i funkciju imunoloških stanica [68].
Nedavno je otkriveno da ljudski SLFN5 može inhibirati ZEB1 transkripciju izravnim vezanjem na SLFN5 vezni motiv na ZEB1 promotoru, čime se održava morfologija epitelnih stanica i inhibiraju metastaze u BRCA mutiranim stanicama raka [69,70]. SLFN5 povećava PTEN smanjivanjem transkripcije ZEB1. Kroz os PTEN/PI3K/AKT/mTOR, povećanje PTEN inhibira rast adenokarcinoma pluća i potiče apoptozu [47].
Iako interakcija SLFN5 sa promotorom ZEB1 u imunološkim stanicama nije potvrđena, ova izvješća sugeriraju ulogu SLFN5 kao multifunkcionalnog modulatora imunoloških stanica. Zanimljivo, SLFN12 inhibira ZEB1; međutim, za razliku od SLFN5, pretpostavlja se da utječe na posttranskripcijsku regulaciju zbog svoje citoplazmatske lokalizacije bez signalne sekvence lokalizacije jezgre. Prekomjerna ekspresija SLFN12 ubrzala je razgradnju proteasoma ZEB1 i usporila translaciju ZEB1 u trostruko negativnim stanicama raka dojke [9].

6. SLFN5, dvosjekli mač u IFN terapiji
Neke zloćudne bolesti mogu se liječiti IFN terapijom u kombinaciji s kemoterapijom i zračenjem. Hematološki zloćudni tumori i limfomi mogu se liječiti ovim terapijskim pristupom [71]. Rekombinantni IFN 2b daje se pacijentima s recidivima melanoma [72]. Hepatitis B i hepatitis C liječe se IFN-om i drugim antivirusnim lijekovima, obično u kombinaciji [73,74]. Antikancerogeni učinci IFN-ova tipa I postali su opsežno prepoznati u posljednjim desetljećima, posebice njihova uključenost u posredovanje interakcija između tumora i imunološkog sustava.
U mišjem malignom melanomu i karcinomu bubrežnih stanica, IFN potiče ekspresiju Slfn1, Slfn2, Slfn3, Slfn5 i Slfn8. Gubitak Slfn2, Slfn4 ili Slfn5 povećao je proliferaciju stanica i maligni rast neovisan o usidrenju, dok je smanjio antiproliferativni učinak IFN-a, što ukazuje na ključnu ulogu Schlafensa u tumorigenezi i kontroli rasta neoplastičnih stanica [75].
Sva ljudska ekspresija Schlafen mRNA inducirana je u normalnim melanocitima terapijom IFN-om, dok je samo SLFN5 induciran u stanicama malignog melanoma i stanicama karcinoma bubrežnih stanica [8,40]. Kada se stanice melanoma stimuliraju IFN-om, ekspresija SLFN5 se znatno povećava, smanjujući proliferaciju stanica raka. Nasuprot tome, smanjenje SLFN5 povećalo je sposobnost melanoma da formiraju kolonije, čak i u prisutnosti IFN-a [40].
Ovo sugerira potencijalnu ulogu SLFN5 u antikancerogenim učincima IFN-a. Međutim, SLFN5 također potencijalno smanjuje antikancerogeni učinak IFN-a u stanicama raka glioma transkripcijskom ko-represijom IFN-ovih odgovora posredovanih STAT1-, za razliku od njegove korisne uloge u melanomu i karcinomu bubrežnih stanica [65]. Smanjenje SLFN5 dovodi do povećane stanične osjetljivosti na antiproliferativne odgovore izazvane IFN-om u stanicama glioblastoma, što implicira da SLFN5 djeluje kao negativni regulator odgovora IFN-a u stanicama raka glioma [65].
Stoga, buduće terapijsko ciljanje SLFN5 u zloćudnim bolestima može zahtijevati preciznu analizu drugih povezanih čimbenika, a dizajn terapeutskog ciljanja određenog tumora može biti potreban za selektivno ciljanje SLFN5.
7. Funkcije Viral Schlafena
Prisutnost intaktnih v-Slfn ORF-ova u nekim OPV-ovima sugerira da se može sačuvati za kritičnu funkciju. Iako postoji nekoliko istraživanja o funkciji v-Slfn, prijavljena su relativno detaljna in vitro i in vivo istraživanja v-Slfn iz CMLV. Ekspresija ovog gena potvrđena je 2 sata nakon infekcije CMLV-om i izražena je u ranoj fazi infekcije neovisno o replikaciji virusne DNA [35].
Za razliku od mišjeg Slfn1, ekspresija CMLV v-Slfn ne utječe na proliferaciju mišjih fibroblasta. Smatra se da je to zbog nedostatka sličnosti između prvih 27 aminokiselina mišjeg Slfn1 i v-Slfn, regije koja je neophodna za inhibiciju rasta fibroblastnih stanica posredovanu mišjim Slfn1-. Kada je protein CMLV v-Slfn eksprimiran u VACV bez intaktnog v-Slfn, nije utjecao na replikaciju rekombinantnog virusa ili morfologiju plaka [35].
Dodatno, intradermalna infekcija miševa ovim rekombinantnim VACV-om nije utjecala na veličinu kožnih lezija [35]. Međutim, u miševa s intranazalnom infekcijom v-Slfn je izazvao manji gubitak težine i brži oporavak u usporedbi s kontrolnim skupinama. Tri dana nakon in vivo infekcije, titar virusa bio je isti kao u kontrolnoj skupini, ali nakon sedam dana opaženo je slabljenje posredovano v-Slfn.
Ovo sugerira da ekspresija v-Slfn ne sprječava replikaciju virusa, već ubrzava čišćenje virusa od strane imunološkog sustava. Ovo je u skladu s opažanjem da je rekombinantni virus koji nosi v-Slfn bio odgođen u širenju u slezenu i da je brže uklonjen iz ovog organa. Dodatno, opsežnije regrutiranje limfocita u zaraženo plućno tkivo opaženo je u prisutnosti ekspresije v-Slfn, iako su te stanice bile manje aktivirane. Visoko virulentni virusi mogu brzo nadvladati svog domaćina, ograničavajući prijenos virusa. Ideja da v-Slfn može smanjiti virulentnost poksvirusa, omogućujući virusu da se odgovarajuće širi u populaciji domaćina, je uvjerljiva [35].
Nedavno je otkrivena nova značajka v-Slfn u poksvirusima (Slika 1). Ciklička GMP-AMP sintaza (cGAS) otkriva citosolnu DNA tijekom virusne infekcije i inducira antivirusno stanje. cGAS aktivira stimulator gena interferona (STING) sintetizirajući drugi glasnik, ciklički GMP-AMP (cGAMP) [76-78]. S otkrićem virusne cGAMP nukleaze nazvane Poxin (poxvirus immune nuclease), imunomodulacijski potencijal poxvirusa dobio je novu perspektivu [6].
Nedavne studije su pokazale da Poxin, koji je domena v-Slfns, može degradirati cGAMP i potreban je za izbjegavanje aktivacije cGAS-STING [79-81]. Otkriveno je da je poxin proizvod VACV gena B2R. Ovaj gen je također poznat kao p26 u entomopoksvirusima i bakulovirusima [80]. Većina ortopoksvirusa uključuje v-Slfn protein sastavljen od dvije domene koje su evoluirale iz različitih izvora. Prema analizi aminokiselinske sekvence, domena koja podsjeća na sekvencu p26 bakulovirusa fuzionirana je na N-završetak v-Slfn domene slične mišjem kratkom obliku Schlafen [35]; ova p26-slična domena je Poxin, cGAMP nukleaza. VACV, u kojem je aktivnost poksina prvi put prijavljena, ne zadržava netaknuti v-Slfn. Gubitak poksina rezultirao je značajnim smanjenjem replikacije VACV in vivo [80].
Važnost sebe, koja uključuje domenu poksina, opsežno je proučavana kod virusa ektromelije (ECTV), koji uzrokuje mišje boginje. Poxin domena, ali ne Slfn-slična domena, bila je dovoljna za inhibiciju cGAS-STING signalizacije s cGAMP nukleaznom aktivnošću na način usporediv sa fuzijom Poxin-Schlafen-slične domene pune duljine. Ovo sugerira da domena ECTV poksina čuva puni potencijal v-Slfn da spriječi aktivaciju DNA senzora preko cGASSTING osi [79].
U nekoliko mišjih modela infekcije, replikacija ECTV-a bez v-Slfn bila je značajno oslabljena, a miševi su pokazali snažan IFN odgovor [79]. Fuzija domene v-Slfn nalik na Poxin-Schlafen visoko je očuvana među ortopoksvirusima, kao što su ECTV, CMLV i novi zoonotski virus majmunskih boginja, što ukazuje na važnost aktivnosti cGAMP nukleaze.
Uloga Slfn-slične domene u aktivaciji Poxina nije jasna. Poxin je zadržao svoju aktivnost cGAMP nukleaze u odsutnosti domene slične Slfn. Unatoč tome, ostaje potrebno istražiti zašto je Slfn-slična domena očuvana u mnogim OPV-ovima. S obzirom na gore spomenuto opažanje da je virulencija himernih virusa smanjena dodavanjem Slfn-slične domene CMLV VACV-u, vjerojatna je hipoteza da reguliranje virusne virulencije može doprinijeti stvaranju povoljnih uvjeta za širenje virusa u prirodi.

8. Schlafens kao antivirusni restrikcijski čimbenici
Antivirusni restrikcijski čimbenici su stanični proteini domaćina koji djeluju kao prva linija obrane, sprječavajući replikaciju i širenje virusa. Restrikcijski faktori prepoznaju patogene i ometaju specifične korake u ciklusu virusne infekcije. Jedinstvena svojstva restrikcijskih faktora koji služe za ograničavanje virusa u ranim fazama uključuju konstitutivnu ekspresiju, samodostatnu aktivnost i trenutno djelovanje [82]. Faktori ograničenja povremeno se povećavaju kao odgovor na IFN. Iako mnogi tipovi stanica konstitutivno izražavaju restrikcijske faktore na niskim razinama potrebnim stanicama u odsutnosti invazije patogena, učinkovita kontrola patogena često zahtijeva indukciju restrikcijskih faktora kao odgovor na infekciju [83]. Budući da Schlafen pripada skupini ISG-a čija je ekspresija povišena kao odgovor na virusnu infekciju ili stimulaciju s različitim molekularnim obrascima povezanim s patogenima (PAMP) [36-39], pretpostavljeno je da mogu imati antivirusno djelovanje.
Uz otkriće staničnih bioloških funkcija Schlafensa tijekom posljednjeg desetljeća, također su otkrivene interakcije s virusima. U ovom odjeljku opisujemo poznate antivirusne funkcije Schlafensa, pregledavajući ih kronološkim redoslijedom kojim su prijavljene (Slika 2). Razjašnjeni su mehanizmi imunološke evazije pomoću kojih virusi antagoniziraju mnoge restrikcijske čimbenike. Nadalje, u skladu s temom da virusi mogu antagonizirati restrikcijske čimbenike kao dio mehanizama imunološke evazije, postoje neki nedavno prijavljeni primjeri virusnih strategija za suzbijanje antivirusnog djelovanja Schlafensa.

Zabilježeno je da Schlafens koji pripadaju različitim skupinama imaju različite uloge, tijekom infekcije, s mnogim virusima. Postoje neki dokazi da neispravnost mišjeg Slfn2 skupine I predisponira stanice za virusnu infekciju u smislu stečenog imuniteta [55]. Grupa II SLFN12 je kandidat za antivirusni čimbenik protiv virusa vezikularnog stomatitisa i raznih retrovirusa, uključujući HIV-1, virus zarazne anemije konja (EIAV), ljudski endogeni retrovirus tipa K (HERK-V), virus mišje leukemije (MLV), i pjenasti virus primata (PFV) [84,85]. Međutim, nedostaju studije o interakciji ovih kratkih ili srednjih oblika Schlafens-a s virusima, a većina studija do sada bila je usredotočena na antivirusnu funkciju Schlafens-a skupine III. Stoga je ključno istražiti igra li C-terminalna proširena domena Schlafensa značajnu ulogu u njihovoj intrinzičnoj funkciji restrikcijskog faktora.
8.1. Uloge SLFN11 tijekom virusne infekcije
Ljudski SLFN11 prvi je put prijavljen 2012. kao snažan inhibitor virusa humane imunodeficijencije 1 (HIV-1) koji ometa proizvodnju virusnih proteina [18]. Otkrili su ga Li i sur. da SLFN11 veže prijenosne RNA (tRNA) i suzbija proizvodnju proteina selektivno ovisno o upotrebi kodona [18]. Daljnja istraživanja otkrila su da konjski SLFN11 inhibira stvaranje EIAV-a mehanizmom sličnim onom koji koristi ljudski SLFN11 [23]. Sustavno istraživanje ciklusa replikacije HIV-a pokazalo je da SLFN11 ne utječe na obrnutu transkripciju, integraciju ili stvaranje i nuklearni izvoz virusne RNA, niti ometa pupanje ili oslobađanje virusnih čestica. Umjesto toga, otkriveno je da inducira selektivnu inhibiciju sinteze virusnih proteina.
Iskorištavanjem određene pristranosti virusnog kodona na A/T nukleotidu, SLFN11 funkcionira u trenutku proizvodnje virusnog proteina. Iako je antivirusni učinak SLFN11 bio sličan onom drugih virusa s neuobičajenim kodonom, poput gripe, nije bio učinkovit protiv adenoasociranog virusa ili herpes simplex virusa (HSV). Ova otkrića su pokazala da je SLFN11 vrlo učinkovit restrikcijski faktor induciran interferonom za retroviruse, kao što je HIV, koji posreduje u antivirusnim učincima putem diskriminacije korištenja kodona [18]. Ovo intrigantno otkriće može djelomično objasniti prethodno uočenu IFN supresiju sinteze specifične za virusne proteine u stanicama zaraženim HIV-om [18,86]. Također naglašava kako imunološki sustav može iskoristiti moguće razlike između sebe i onih koji nisu za stanice domaćina kako bi ciljao i eliminirao viruse. Čini se da ne postoji preferencija za tip tRNA u vezivanju SLFN11 na tRNA [18].
Bit će potrebno provesti biokemijske eksperimente kako bi se otkrilo kako SLFN11 modulira funkciju tRNA i utječe na upotrebu kodona specifičnog za virus. SLFN11 je visoko eksprimiran, ne samo u CD4 plus T stanicama već i u monocitima i moDC [37,87]. Poznato je da su CD4 plus T stanice primarni rezervoar za latentnu HIV infekciju, a latencija HIV-a također se može uspostaviti u monocitima i makrofagima [88]. Stoga se smatra da visoka ekspresija SLFN11 u tim stanicama ima ulogu u latentnoj infekciji HIV-om i može biti ključna komponenta urođenog imunološkog odgovora na HIV.
Nedavno je otkriveno da se mišji Slfn2 veže na tRNA i inhibira njezinu razgradnju u okruženju oksidativnog stresa [89]. Iako je ova studija pokazala da je Slfn2 inhibirao infekciju mišjim citomegalovirusom (MCMV), rezultat je bio posljedica adaptivnog imuniteta posredovanog T-stanicama [89]. Unatoč tome, ova opažanja zaslužuju temeljito ispitivanje interakcije između tRNA modulacije Slfn2 i mišjih retrovirusa, kao i paralela i razlika s ljudskim SLFN11. Budući da je N-terminalni dio SLFN11 uključen u vezanje tRNA, mogu postojati evolucijske sličnosti u sekvenci s kratkim oblikom Slfn2. Dodatno, otkriće da SLFN13 i SLFN14 sudjeluju u modulaciji tRNA otvara put za buduća istraživanja kako bi se utvrdilo dijele li Schlafens zajedničke funkcije u biologiji tRNA [24,90].
Budući da dolazni virusni genom jednolančanih RNA virusa pozitivnog smisla zahtijeva neposrednu translaciju kako bi se omogućila replikacija, ti su virusi posebno osjetljivi na učinke SLFN11 na sintezu proteina. To je dokazano u rodu Flavivirusa, uključujući virus Zapadnog Nila (WNV), virus denge (DENV) i virus Zika (ZIKV) [21]. Postoje sličnosti i razlike u mehanizmu djelovanja Schlafenovih proteina protiv flavivirusa i lentivirusa. N-terminalni dio SLFN11 bitan je i dovoljan za antivirusno djelovanje, budući da sprječava virusom inducirane promjene u tRNA repertoaru zaraženih stanica. Za razliku od WNV infekcije, koja je zahvatila samo podskup tRNA u stanicama s nedostatkom SLFN11- [21], HIV-1 je povisio ukupne razine tRNA u odsutnosti SLFN11 [18].
Sposobnost SLFN11 da regulira obilje tRNA pulova mogla bi biti povezana s osjetljivošću stanica na agense koji oštećuju DNA. Nekoliko je studija otkrilo da su stanice raka s višom ekspresijom SLFN11 ranjivije na agense koji oštećuju DNA [12,33,91,92]. Više razine SLFN11 mogu ograničiti broj određenih tRNA koje utječu na translaciju proteina za popravak DNA kodiranih otvorenim okvirima čitanja s predrasudama kodona, kao što su ATM i ATR [93]. Osim toga, SLFN11 nepovratno inhibira replikaciju DNA na mjestima oštećenja DNA na način ovisan o C-terminalnoj domeni helikaze [34,94]. Poznato je da različiti virusi iskorištavaju proteine uključene u reakciju stanica domaćina na oštećenje DNA za njihovu učinkovitu replikaciju [95].
Uključenost proteina za kontrolu oštećenja DNA ATM i ATR u infekciju HIV-om opsežno je proučavana. ATM ima pozitivan učinak na kasnu ekspresiju gena HIV-a i funkciju Rev, virusnog posttranskripcijskog regulatora [96]; u međuvremenu, aktivnost ATR kinaze je potrebna kako bi se dovršio proces integracije virusne DNA i podržalo preživljavanje transduciranih stanica [97]. Kod ZIKV infekcije, ATM signalni put povećava replikaciju virusa [98]. Ova otkrića sugeriraju da bi Schlafens trebalo dodatno istražiti u smislu otpornosti stanica domaćina na viruse koji povoljno iskorištavaju odgovore na oštećenje DNK kako bi se osigurala učinkovita replikacija.
ZIKV je posljednjih godina izazvao široku zabrinutost zbog svoje sposobnosti da izazove abnormalnosti pri rođenju kod dojenčadi i Guillain-Barréov sindrom kod odraslih. ZIKV se može prenijeti spolnim putem, preživjeti u muškom reproduktivnom sustavu [99], a kod žena proći kroz placentu i zaraziti fetus [100]. Dostupne su ograničene informacije o učincima ZIKV-a na reproduktivno zdravlje i plodnost. S obzirom da se SLFN11 ne eksprimira u placenti ili testisima [22], potrebna su dodatna istraživanja kako bi se otkrilo je li također povezan s prenatalnim i spolno prenosivim infekcijama.
Gen SLFN11 evoluirao je uz ponavljanu pozitivnu selekciju u primata [22]. Nadalje, antivirusna učinkovitost SLFN11 bila je najveća kod vrsta primata koji nisu ljudi, kao što su giboni i marmozeti, ali manje učinkovita kod ljudi i bonobo vrsta koje su evolucijski bliske ljudima, što ukazuje da su učinci SLFN11 postali vrlo specifični za vrstu tijekom vremena [22]. SLFN11 je funkcionalan u odsutnosti infekcije i smanjuje proizvodnju proteina iz određenih transkripata domaćina [18,93]. To implicira da SLFN11 općenito može inhibirati sintezu proteina iz transkripata koji nisu optimizirani za kodon, čime unaprijed uspostavlja nepovoljno stanično okruženje za sintezu virusnog proteina.
Virusi su razvili načine koji se suprotstavljaju restrikcijskim faktorima domaćina. Iako je dokazan trend smanjenja SLFN11 proteina u HCMV-inficiranim stanicama [101], virusni antagonisti za SLFN11 nisu otkriveni mnogo godina. Međutim, nedavno je dokazan antivirusni učinak SLFN11 i njegov virusni antagonistički mehanizam na HCMV [102]. Kasno eksprimirani protein RL1 HCMV cilja SLFN11 za razgradnju proteasoma i prvo je otkriće virusnog antagonista ovog restrikcijskog faktora. U ovoj studiji otkriveno je da je stanični kompleks ubikvitin ligaze CRL4 E3 dodatno uključen u razgradnju SLFN11 pomoću RL1 [102].
Iako SLFN11 ima značajan utjecaj na replikaciju HIV-a, WNV-a i ZIKV-a, ti se virusi još uvijek mogu replicirati u stanicama koje izražavaju SLFN11. U usporedbi s drugim flavivirusima ili HIV-om, replikacija DENV-a značajno je smanjena ekspresijom SLFN11 [21]. Ovo sugerira da je DENV osjetljiviji od drugih virusa na učinke SLFN11. Stoga bi se očekivalo da DENV-u nedostaje antagonistički mehanizam za SLFN11, dok WNV, ZIKV i HIV-1 mogu posjedovati prikrivene antagonističke mehanizme.
Prijavljen je mehanizam kojim fosforilacija SLFN11 pomoću katalitičke podjedinice G proteinske fosfataze 1 (PPP1CC) regulira sposobnost cijepanja tRNA tipa II [103]. Dobro je poznato da aktivnost staničnih proteina reguliraju virusne kinaze [104]. Još uvijek nisu pronađeni dokazi koji bi poduprli hipotezu da virusi reguliraju fosforilaciju SLFN11 putem kinaza kodiranih virusom ili neizravno putem kinaza stanica domaćina, kao što je PPP1CC. Potrebna su daljnja istraživanja kako bi se istražila mogućnost da virusi iskorištavaju fosforilaciju proteina kako bi zaobišli antivirusnu aktivnost Schlafensa, kao što je primijećeno za druge restrikcijske čimbenike domaćina [105-112].
8.2. Uloge SLFN13 tijekom virusne infekcije
Kristalografska analiza otkrila je da je SLFN13 nova klasa tRNA/rRNA nukleaza [24]. Osim toga, također je objavljeno da SLFN13 ima antivirusnu funkciju protiv HIV-a i ZIKV-a inhibicijom sinteze proteina putem nukleolitičke aktivnosti, slično SLFN11. Međutim, ključna determinanta cijepanja tRNA pomoću SLFN13, koji blokira sintezu proteina, je sekundarna struktura tRNA i nije u korelaciji s anti-kodonskom sekvencom [24], koja se, čini se, razlikuje od mehanizma koji se temelji na upotrebi kodona. SLFN11.
Sekvenca N-terminalne domene SLFN13, koja je potrebna za funkciju enzima, sačuvana je u drugim Schlafenovim proteinima. Međutim, specifični pozitivno nabijeni aminokiselinski ostaci su različiti. Potvrđeno je da određeni članovi obitelji, kao što su ljudski SLFN5 i mišji Slfn1, nisu uključeni u cijepanje tRNA [24]. Stoga je vjerojatno da distribucija pozitivno nabijenih aminokiselinskih ostataka unutar N-terminalne domene može odrediti sposobnost i tendencije selekcije cijepanja tRNA/rRNA kao i antivirusne spektre za druge Schlafens.
Uočeno je da infekcije virusom influence A (PR8) i B (Victoria) induciraju ekspresiju mRNA SLFN13 u stanicama A549 adenokarcinoma ljudskih pluća [19]. Ova je indukcija bila snažnija u virusnoj mutantnoj infekciji s nedostatkom NS{4}}, vjerojatno zbog sposobnosti NS1 da potisne RIG-I-posredovanu aktivaciju IFN promotora [113]. Nadalje, smanjenje SLFN13 povećalo je razvoj plaka virusa influence A i B, što implicira da SLFN13 potiče antivirusne odgovore na te viruse [19]. Međutim, nije poznato je li antivirusna funkcija SLFN13 protiv virusa influence povezana s cijepanjem tRNA/rRNA. Stoga postoji potreba za utvrđivanjem je li nukleolitička aktivnost Schlafena uobičajeni mehanizam za antivirusnu funkciju posredovanu Schlafenom. Nepostojanje antivirusnog učinka SLFN11 protiv virusa s genomom jednolančane RNA negativnog smisla [21] sugerira postojanje mehanizma neovisnog o funkciji SLFN13 protiv virusa influence.
8.3. Uloge SLFN14 tijekom virusne infekcije
Za SLFN14 također je prijavljeno antivirusno djelovanje, a ekspresija se povećava infekcijom virusom influence A [19]. Smanjenje SLFN14 ograničilo je regulaciju IP-10, glavnog ISG-a, nakon infekcije gripom. Ovi rezultati sugeriraju mogući mehanizam kojim SLFN14 prepoznaje virusni RNA genom, pojačava aktivirajući RIG-I posredovani signal i inhibira replikaciju influence [19]. Međutim, potrebno je potvrditi da li SLFN14, kao i helikaze, poput DDX1 ili RIG-I, doista detektira virusni genom [114]. SLFN14 odgađa nuklearnu translokaciju nukleoproteina NP. Odgođena nuklearna translokacija NP može oslabiti virusnu replikaciju ometanjem nuklearnog transporta virusnog ribonukleoproteina.
Osim njegovih učinaka na RNA viruse, SLFN14 također je dokazano da posjeduje antivirusno djelovanje protiv DNA virusa, kao što je virus varicella-zoster (VZV). Infekcija VZV inducira ekspresiju SLFN14 i inhibira proizvodnju virusnog antigena u stanicama koje prekomjerno eksprimiraju SLFN14 [19]. Iako se pretpostavlja da je antivirusni mehanizam SLFN14 protiv RNA virusa i DNA virusa različit, za detaljniju analizu mehanizma potrebno je dodatno istraživanje navodne domene helikaze SLFN14 i povezanosti IFN signalizacije posredovane RIG-I. Osim toga, budući da su vrste stanica koje eksprimiraju SLFN14 vrlo ograničene ili je razina ekspresije niska [115], stvarnu funkciju SLFN14 u stanicama zaraženim virusom tek treba procijeniti.
Utvrđeno je da SLFN14 ima aktivnost endonukleaze povezanu s ribosomima i može razgraditi tRNA, rRNA i mRNA [90]. Ne postoji specifičnost sekvence ili specifičnost poželjne strukture u cijepanju RNK, a ova enzimska aktivnost strogo je ovisna o Mg2 plus - i Mn2 plus i neovisna o ATP [90]. Međutim, samo C-terminalno skraćena kratka verzija SLFN14 pokazala je enzimsku aktivnost, dok SLFN14 pune duljine nije imao aktivnost endonukleaze i nije se vezao na ribosome [90]. Čini se da je ova značajka način održavanja integriteta staničnih RNA. Budući da je protein SLFN14 prisutan na niskim razinama u većini stanica i javlja se u jezgri, stanje neaktivnog prekursora slično kaspazi može zaštititi stanične RNA od aktivnosti nespecifične endonukleaze. Virusne infekcije induciraju ekspresiju SLFN14 poput ekspresije RNaze L [116], i može sudjelovati u čišćenju ukupne stanične RNK radi inhibicije reprodukcije virusa. Međutim, i dalje je potrebno dokazati da se SLFN14 prerađuje u aktivni oblik nakon infekcije ili u određenim okruženjima.
8.4. Uloge SLFN5 tijekom virusne infekcije
U ljudskim stanicama, SLFN5 je, uz SLFN11, najzastupljeniji protein obitelji Schlafen [18]. SLFN5 je nuklearni član obitelji Schlafen, koji je povezan s proliferacijom i diferencijacijom imunoloških stanica [28,117].
Studije pokazuju da infekcija virusom influence, WNV-om i rinovirusom dovodi do povećane ekspresije SLFN5 [37,118,119]. Međutim, funkcija SLFN5 protiv ovih virusa nije istražena, a za razliku od SLFN11, eksperimentalno je utvrđeno da SLFN5 nema antivirusno djelovanje protiv HIV infekcije [18]. Nedavno istraživanje SLFN5 otkrilo je antivirusno djelovanje i mehanizam protiv HSV-1, virusa s dvolančanim DNA genomom [20]. U toj studiji, faktori domaćina povezani s HSV-1 DNA izolirani su proteomičkom tehnikom nazvanom Isolation of Proteins On Nascent DNA (iPOND), koja identificira proteine koji se nakupljaju na novosintetiziranoj DNA [120-122]. Kada se primijeni na infekciju HSV-1 divljim tipom i mutiranim virusima, ova tehnika je otkrila da SLFN5 prolazi proteasomalnu degradaciju kao rezultat ubrzane ubikvitinacije virusnim proteinom ICP0.
HSV{{0}} neposredno-rani protein ICP0 olakšava transkripciju virusnog gena i reaktivaciju virusa iz latencije. ICP0 ima domenu ubikvitin E3 ubikvitin ligaze koja antagonizira obranu domaćina kroz proteasomalnu degradaciju intrinzičnih antivirusnih faktora domaćina [123,124]. Utvrđeno je da je DNK HSV-1 povezana s nekoliko ciljeva razgradnje ICP{{10}}, za koje se također pokazalo da inhibiraju proizvodnju virusnih gena i/ili aktivaciju antivirusnih staničnih signala [124]. ]. Iako su prethodne studije identificirale ICP0 supstrate kao restrikcijske faktore, mehanizam za suzbijanje ekspresije virusnog gena nije u potpunosti shvaćen. U ovoj nedavnoj studiji biokemijski je potvrđeno da ICP0 specifično ubikvitinira i razgrađuje SLFN5 putem proteasoma [20].
Utvrđeno je da se izravna interakcija između ICP{{0}} i SLFN5 odvija preko proširene C-terminalne domene SLFN5, regije koja je odsutna u SLFN11, a koja nije bila ciljana za razgradnju. C-terminalna regija SLFN5 sadrži intrinzički poremećenu regiju, čestu značajku staničnih proteina vezanih virusnim faktorima, kao što je ICP0 [125]. Antivirusni učinak SLFN5 na HSV-1 jasnije je uočen kod mutantnih virusa kojima nedostaje E3 ligazna aktivnost ICP0 nego kod virusa divljeg tipa. Zapažanja da HSV-1 cilja SLFN5 [20], a HCMV cilja SLFN11 [102] sugeriraju da bi razgradnja posredovana proteasomom mogla biti češća virusna strategija koja se koristi za antagoniziranje Schlafenove restrikcije.
Predloženo je da se antivirusni mehanizam SLFN5 veže na virusnu DNA i inhibira učitavanje RNA polimeraze II na promotore virusnog gena [20]. Dodatno, dokazano je da, za razliku od ostalih Schlafena, nije utjecao na razgradnju mRNA. Iako pretpostavljena aktivnost helikaze može biti mehanizam kojim SLFN5 potiskuje transkripciju gena virusne DNA, motiv Walker A helikaze SLFN5 ne utječe na njegovu antivirusnu funkciju [20]. Čini se da SLFN5 nema nikakvu specifičnost DNK sekvence. Ispitivanje vezanja SLFN5 na promotor i regije tijela gena nije otkrilo nikakvu vidljivu preferenciju; međutim, postojala je primjetna tendencija da se više vežu na virusnu DNA nego na staničnu DNA [20]. Nedavna studija strukture SLFN5 pokazala je visok afinitet za dvolančanu DNA i identificirala ostatke uključene u vezanje nukleinske kiseline [31]. Iako SLFN5 veže tRNA, ne dijeli aktivnost endoribonukleaze zabilježenu za druge Schlafens [31]. Također se pokazalo da SLFN5 ima prednost pri vezanju na slobodnu DNA u odnosu na DNA vezanu na nukleosom [31]. Možda lakoća pristupa eukromatskoj virusnoj DNK u okruženju litičke infekcije može pridonijeti selektivnom vezanju na virusnu genomsku DNK [126].
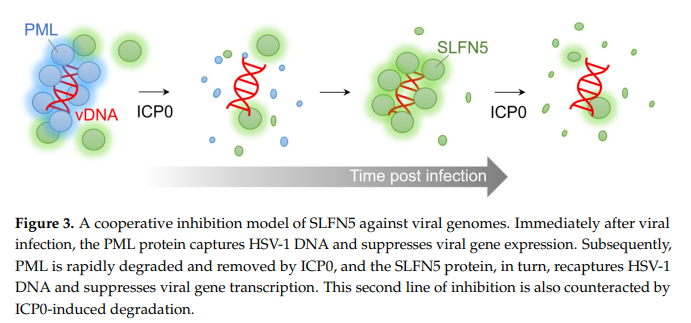
Interakcija između SLFN5 i virusne DNA otkrivena je i za dolazne virusne genome i za aktivno replicirane virusne genome u odjeljcima virusne replikacije [20]. Protein PML domaćina, dobro poznati HSV{3}} restrikcijski faktor, kao i ICP0 supstrat, također pristupa dolaznoj virusnoj DNK i inhibira transkripciju virusnog gena [127-130]. Iako su potrebna daljnja biokemijska istraživanja, čini se da je razgradnja SLFN5 posredovana ICP-om manje učinkovita od razgradnje PML-a [20]. Neposredno nakon infekcije, većina HSV-1 DNA okružena je PML proteinom; međutim, kada dođe do ekspresije ICP0, PML se brzo eliminira, a virusna DNA ponovno biva zarobljena proteinom SLFN5 [20].
Ovo sugerira da bi PML i SLFN5 mogli surađivati kako bi stvorili nepovoljno okruženje za ekspresiju virusnih gena. Stoga bi uloga SLFN5 mogla biti druga linija obrane koja podupire antivirusnu funkciju PML-a (Slika 3). Opažanje da SLFN5 regulira imunološki odgovor, a također je na meti ICP0, sugerira da bi mogao biti dio 'samočuvanog' imunološkog puta za praćenje infekcije. Razgradnja SLFN5 pomoću ICP0 mogla bi stoga potaknuti aktivaciju sekundarnih imunoloških odgovora. Ova zaštitna hipoteza nedavno je predložena za MORC3, drugu metu ICP0 [131]. Potrebne su daljnje studije kako bi se razumjele veze između SLFN5 i drugih regulatora infekcije HSV-1.
Nedavna analiza jednostaničnog transkriptoma HSV-1 otkrila je da je za ekspresiju gena HSV-1 potrebno regrutiranje -katenina u odjeljak za replikaciju virusa [132]. Poznato je da SLFN5 inhibira migraciju i proliferaciju stanica inhibiranjem ekspresije katenina [133,134], što implicira da SLFN5 također može neizravno utjecati na ekspresiju gena HSV-1.
Iako SLFN5 nema antivirusno djelovanje protiv retrovirusa, ima antivirusni učinak protiv HSV-2, alphaherpesvirinae bliskog HSV-1. Zanimljivo je da su se rezultati za betaherpesvirinae HCMV razlikovali ovisno o stadiju infekcije [20]. Unutar prva 24 sata nakon infekcije, smanjenje SLFN5 potiče ekspresiju virusnih neposrednih ranih i ranih transkripata gena; međutim, to se poništava u kasnoj fazi, što rezultira smanjenom ekspresijom ovih virusnih gena u odsutnosti SLFN5. Kao rezultat toga, prinos replikacije HCMV-a blago je smanjen u stanicama s nedostatkom SLFN5-. Jedna razlika između HSV-1 i HCMV je vremenski tijek infekcije, pri čemu je replikacija HSV-1 puno brža od HCMV-a.
Budući da SLFN5 inhibira transkripciju ISG-a posredovanu STAT1- [65], smanjenje SLFN5 može rezultirati pojačanom ISG signalizacijom, što smanjuje replikaciju HCMV-a. Doista, obaranje SLFN5 rezultiralo je višim razinama ekspresije ISG15, koje su se dodatno povećale nakon HCMV infekcije [20]. Kao rezultat toga, SLFN5 je izravno uključen u smanjenje rane ekspresije virusnog gena i čini se da ima poseban učinak na HSV-1 u kasnijim fazama. Drugi DNA virus, adenovirus, nije bio pod utjecajem SLFN5, a virusna infekcija nije rezultirala razgradnjom proteina SLFN5 [20]. Zajedno, ovi podaci sugeriraju specifičnost antivirusne aktivnosti u obitelji proteina Schlafen, slično onome što je primijećeno za druge obitelji restrikcijskih faktora domaćina.
9. Zaključci i buduće perspektive
Kontinuirano i dubinsko istraživanje obitelji Schlafen posljednjih je godina postiglo značajan napredak prema razjašnjavanju uloge proteina Schlafen. Aktualne studije su pokazale da Schlafen proteini igraju ključnu ulogu u regulaciji i imunološkog odgovora i staničnog ciklusa. Neki od tih proteina povezani su s osjetljivošću na liječenje tumora i rezistencijom na lijekove [13-15,135]; stoga biološka funkcija proteina obitelji Schlafen u tumorskim stanicama pruža nove metode i ideje za otkrivanje i liječenje tumora. Osim toga, Schlafenovi proteini pokazuju relativno širok inhibicijski učinak na retroviruse putem RNA modulacije za inhibiciju translacije. Schlafen proteini također su uključeni u virusnu infekciju neizravno putem interferonske signalizacije. Otkriće mehanizma za izravnu inhibiciju ekspresije virusnog gena putem vezanja SLFN5 na virusnu DNA u jezgri istaknulo je potencijalnu raznolikost u antivirusnim mehanizmima obitelji Schlafen.
Brojna otkrića do danas pokazuju da obitelj Schlafen ima ulogu u različitim staničnim odgovorima, uključujući razvoj imunoloških stanica i intrinzični/urođeni imunitet. Ova obitelj proteina je, nedvojbeno, važna meta za liječenje raka, kao i istraživanja u razumijevanju i prevenciji virusnih infekcija. Međutim, funkcionalne studije Schlafenovih proteina još su u povojima i mnoga važna pitanja tek treba riješiti. Iako obitelj Schlafen dijeli nekoliko sličnih domena, one pokazuju funkcionalne razlike. Ove razlike impliciraju da članovi obitelji Schlafen pridaju specifičnost svojim antivirusnim aktivnostima, naglašavajući važnost proučavanja strukturnih svojstava i funkcionalnih mehanizama.
Srećom, utvrđene su strukture za štakorski Slfn13 [24] i ljudski SLFN5 [31], dajući uvid u tekuće studije proteina obitelji Schlafen. Nadalje, ograničenja pokusa na životinjama za kliničku primjenu moraju se prevladati. Obitelj Schlafen pokazala je brzu evolucijsku tendenciju kod nekoliko glodavaca, a stupanj očuvanosti Schlafen gena glodavaca i ljudi nije visok. Na primjer, SLFN5 i SLFN11 su najzastupljeniji i vrlo proučavani u različitim stanicama, ali sličnost između miševa i ljudi za SLFN5 je samo 59 posto na temelju identiteta sekvence aminokiselina, a ne postoji ortolog SLFN11 u miševa. SLFN5 i SLFN14 jedini su ortolozi koje dijele miševi i ljudi (Slika 1). Stoga postoji potreba za razvojem nove platforme, kao što su modeli organoida, koji mogu zamijeniti in vivo studije.
S obzirom na različite funkcije proteina obitelji Schlafen, očekuje se da različiti proteini partneri vezanja u stanici igraju ulogu u njihovoj regulaciji. Iako nije objavljeno izvješće o rezultatima globalnog proteomskog pristupa interaktomu, ključno je otkriti i proučiti ulogu veznih partnera kao čimbenika koji diferenciraju funkciju i regulaciju unutarstanične aktivnosti proteina obitelji Schlafen. Proučavanje povezanosti između razine ekspresije Schlafena i prognoze raka može se primijeniti na istraživanje tumora posredovano virusom ili liječenje pomoću virusnih vektora. Unatoč svom nazivu, polje Schlafen daleko je od uspavanog. Studije koje su u tijeku pružit će važan uvid u biologiju virusa i tumora te će predložiti načine na koje se njihove jedinstvene aktivnosti mogu iskoristiti za terapeutske primjene.

Doprinosi autora:
Konceptualizacija, ETK i MDW; pisanje—priprema izvornog nacrta, ETK; pisanje—recenzija i uređivanje, MDW; vizualizacija, ETK Svi su autori pročitali i suglasni s objavljenom verzijom rukopisa.
Financiranje:
Ovaj je rad podržao Program temeljnih znanstvenih istraživanja putem Nacionalne istraživačke zaklade Koreje (NRF) koju financira Ministarstvo obrazovanja (2021R1A2C1010313). MDW je djelomično podržan grantovima Nacionalnog instituta za zdravlje (AI115104 i NS082240) i sredstvima Dječje bolnice u Philadelphiji.
Zahvale:
Zahvaljujemo Joeu Dybasu na njegovim komentarima na rukopis.
Sukob interesa:
Autori izjavljuju da nema sukoba interesa.
Reference
1. Schwarz, DA; Katayama, CD; Hedrick, SM Schlafen, nova obitelj gena za regulaciju rasta koji utječu na razvoj timocita. Imunitet 1998, 9, 657–668. [CrossRef]
2. Geserick, P.; Kaiser, F.; Klemm, U.; Kaufmann, ONA; Zerrahn, J. Modulacija razvoja T stanica i aktivacija novim članovima obitelji Schlafen (slfn) gena koji nose motiv sličan RNA helikazi. Int. Immunol. 2004., 16, 1535–1548. [CrossRef] [PubMed]
3. Neumann, B.; Zhao, L.; Murphy, K.; Gonda, TJ Subcelularna lokalizacija Schlafenove obitelji proteina. Biochem. Biophys. Res. Komun. 2008, 370, 62–66. [CrossRef] [PubMed]
4. Kuang, C.; Yang, T.; Zhang, Y.; Zhang, L.; Wu, Q. Schlafen 1 inhibira proliferaciju i stvaranje cjevčica endotelnih progenitorskih stanica. PLoS One 2014, 9, e109711. [CrossRef] [PubMed]
5. Brady, G.; Boggan, L.; Bowie, A.; O'Neill, LAJ Schlafen-1 uzrokuje zaustavljanje staničnog ciklusa inhibicijom indukcije ciklina D1. J. Biol. Chem. 2005, 280, 30723-30734. [CrossRef]
6. Oh, P.-S.; Patel, VB; Sanders, MA; Kanwar, SS; Yu, Y.; Nautiyal, J.; Patel, BB; Majumdar, APN Schlafen-3 smanjuje ekspresiju markera matičnih stanica raka i autokrinu/juktakrinu signalizaciju u stanicama raka debelog crijeva otpornim na FOLFOX. Am. J. Physiol. Gastrointest. Liver Physiol. 2011, 301, G347-G355. [CrossRef]
7. Patel, VB; Yu, Y.; Das, JK; Patel, BB; Majumdar, APN Schlafen-3: Novi regulator intestinalne diferencijacije. Biochem. Biophys. Res. Komun. 2009, 388, 752–756. [CrossRef]
8. Sassano, A.; Mavrommatis, E.; Arslan, AD; Kroczynska, B.; Beauchamp, EM; Khuon, S.; Chew, T.-L.; Green, KJ; Munshi, HG; Verma, AK; et al. Ljudski Schlafen 5 (SLFN5) je regulator pokretljivosti i invazivnosti stanica karcinoma bubrežnih stanica. Mol. Ćelija. Biol. 2015, 35, 2684–2698. [CrossRef]
9. Al-Marsoummi, S.; Vomhof-DeKrey, E.; Basson, MD Schlafen12 Smanjuje agresivnost trostruko negativnog raka dojke putem posttranskripcijske regulacije ZEB1 koja pokreće diferencijaciju matičnih stanica. Ćelija. Physiol. Biochem. 2019, 53, 999–1014. [CrossRef]
10. Al-Marsoummi, S.; Pacella, J.; Dockter, K.; Soderberg, M.; Singhal, SK; Vomhof-Dekrey, EE; Basson, MD Schlafen 12 je prognostički povoljan i smanjuje C-Myc i proliferaciju u adenokarcinomu pluća, ali ne i u karcinomu skvamoznih stanica pluća. Cancers 2020, 12, 2738. [CrossRef]
11. Companioni Nápoles, O.; Tsao, AC; Sanz-Anquela, JM; Sala, N.; Bonet, C.; Pardo, ML; Ding, L.; Šimo, O.; Saqui-Salces, M.; Blanco, potpredsjednik; et al. Ekspresija SCHLAFEN 5 korelira s intestinalnom metaplazijom koja napreduje do raka želuca. J. Gastroenterol. 2016, 52, 39–49. [CrossRef] [PubMed]
12. Zoppoli, G.; Regairaz, M.; Leo, E.; Reinhold, WC; Varma, S.; Ballestrero, A.; Doroshow, JH; Pommier, Y. Pretpostavljena DNA/RNA helikaza Schlafen-11 (SLFN11) senzibilizira stanice raka na agense koji oštećuju DNA. Proc. Natl. Akad. Sci. SAD 2012, 109, 15030–15035. [CrossRef] [PubMed]
13. Tian, L.; Pjesme.; Liu, X.; Wang, Y.; Xu, X.; Hu, Y.; Xu, J. Schlafen-11 senzibilizira stanice kolorektalnog karcinoma na irinotekan. Antikancerogeno. Lijekovi 2014, 25, 1175–1181. [CrossRef] [PubMed]
14. Nogales, V.; Reinhold, WC; Varma, S.; Martinez-Cardus, A.; Moutinho, C.; Moran, S.; Heyn, H.; Sebio, A.; Barnadas, A.; Pommier, Y.; et al. Epigenetska inaktivacija navodne DNA/RNA helikaze SLFN11 u ljudskom raku daje otpornost na lijekove platine. Oncotarget 2015, 7, 3084–3097. [CrossRef] [PubMed]
15. Stewart, CA; Tong, P.; Cardnell, RJ; Sen, T.; Li, L.; Gay, CM; Masrorpour, F.; Fan, Y.; Bara, RO; Feng, Y.; et al. Dinamičke varijacije u prijelazu epitela u mezenhim (EMT), ATM i SLFN11 upravljaju odgovorom na PARP inhibitore i cisplatin kod karcinoma pluća malih stanica. Oncotarget 2017, 8, 28575–28587. [CrossRef] [PubMed]
16. Shee, K.; Wells, JD; Jiang, A.; Miller, TW. Integrirana ekspresija gena za rak i analiza osjetljivosti na lijekove otkriva SLFN11 mRNA kao solidan tumorski biomarker koji predviđa osjetljivost na kemoterapiju koja oštećuje DNA. PLoS One 2019, 14, e0224267. [CrossRef]
17. Winkler, C.; Armenija, J.; Jones, GN; Tobalina, L.; Sale, MJ; Petreus, T.; Baird, T.; Serra, V.; Wang, AT; Lau, A.; et al. SLFN11 informira o standardu skrbi i novim tretmanima u širokom rasponu modela raka. Br. J. Rak 2021, 124, 951–962. [CrossRef]
18. Li, M.; Kao, E.; Gao, X.; Sandig, H.; Limmer, K.; Pavon-Eternod, M.; Jones, TE; Landry, S.; Pan, T.; Weitzman, MD; et al. Inhibicija sinteze proteina HIV-a ljudskim šlafenom temeljena na upotrebi kodona 11. Nature 2012, 491, 125–128. [CrossRef]
19. Seong, R.-K.; Seo, S.; Kim, J.-A.; Fletcher, SJ; Morgan, NV; Kumar, M.; Choi, Y.-K.; Shin, OS Schlafen 14 (SLFN14) je novi antivirusni čimbenik uključen u kontrolu replikacije virusa. Imunobiologija 2017, 222, 979–988. [CrossRef]
20. Kim, ET; Dybas, JM; Kulej, K.; Reyes, ED; Cijena, AM; Akhtar, LN; Orr, A.; Garcia, BA; Boutell, C.; Weitzman, MD Komparativna proteomika identificira Schlafen 5 (SLFN5) kao restrikcijski faktor virusa herpes simplexa koji potiskuje virusnu transkripciju. Nat. Microbiol. 2021, 6, 234–245. [CrossRef]
For more information:1950477648nn@gmail.com
