Platforme cjepiva na bazi nukleinske kiseline protiv koronavirusne bolesti 19 (COVID‑19)
Aug 11, 2023
Sažetak
Pandemija koronavirusne bolesti 2019. (COVID{1}}) do danas je zarazila 673.010.496 pacijenata i uzrokovala smrt 6.854.959 slučajeva širom svijeta. Uloženi su ogromni napori da se razviju bitno različite platforme cjepiva protiv COVID-19. Cjepiva na bazi nukleinske kiseline koja se sastoje od mRNA i DNA cjepiva (cjepiva treće generacije) obećavaju u smislu brze i prikladne proizvodnje i učinkovitog izazivanja imunoloških odgovora protiv COVID-a-19. Nekoliko temeljenih na DNK (ZyCoV-D, INO-4800, AG0302-COVID19 i GX-19N) i mRNA (BNT162b2, mRNA-1273 i ARCoV) odobrene platforme cjepiva korištene su za prevenciju COVID-19. MRNA cjepiva su na čelu svih platformi za prevenciju COVID-19. Međutim, ova cjepiva imaju manju stabilnost, dok su DNA cjepiva potrebna s višim dozama za stimulaciju imunoloških odgovora. Intracelularna isporuka cjepiva na bazi nukleinskih kiselina i njihovih nuspojava zahtijeva daljnja istraživanja. S obzirom na zabrinjavajuću ponovnu pojavu varijanti COVID-19, ponovna procjena cjepiva i razvoj polivalentnih cjepiva ili pan-koronavirusnih strategija ključni su za učinkovitu prevenciju infekcije.

dobrobiti dodatka cistanche-kako ojačati imunološki sustav
Kliknite ovdje za pregled Cistanche proizvoda za jačanje imuniteta
【Tražite više】 E-pošta:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
Ključne riječi
Koronavirusna bolest 19 · Cjepiva na bazi nukleinske kiseline · Imunitet · Zaštita
Pozadina
Krajem 2019. novi beta koronavirus pojavio se u Wuhanu u Kini i brzo se proširio svijetom. Koronavirusna bolest 2019. (COVID-19) ima veliki potencijal pandemije zbog visoke stope zaraze s visokom smrtnošću na globalnoj razini (Sharma et al. 2020; Su et al. 2020; Wibawa 2021). Stoga su potrebni znatni napori za razvoj učinkovitih cjepiva ili terapija protiv bolesti (Su et al. 2020.). Simptomi bolesti COVID-19 variraju, uključujući blage simptome slične fu, upalu pluća, sindrom akutnog respiratornog distresa (ARDS) i smrtni ishod. Bolesnici s rakom, dijabetesom, kardiovaskularnim bolestima, starije odrasle osobe, pa čak i genetski predisponirane osobe izložene su najvećem riziku od ozbiljnosti COVID-19 (Sharma et al. 2020; Su et al. 2020; Wibawa 2021; Vakil et al. 2022). Prema preporukama Svjetske zdravstvene organizacije (WHO), nošenje maski, korištenje antivirusnih lijekova, socijalno distanciranje i pridržavanje procedura cijepljenja ključna su ponašanja za kontrolu pandemije COVID-19 širom svijeta (Sharma et al. 2020.). Znanstveni napori usmjereni na razvoj učinkovitih cjepiva protiv invazivnih patogena datiraju mnogo godina unatrag (Deb et al. 2020; Zhang et al. 2020; Wibawa 2021). Ove platforme cjepiva također su dizajnirane protiv patogenih bakterija (Farhani et al. 2019; Jafari i Mahmoodi 2021). U tom smislu, razvoj učinkovitog, zaštitnog i sigurnog cjepiva smatra se ključnim preventivnim pristupom za sprječavanje širenja teškog akutnog respiratornog sindroma koronavirusa 2 (SARS-CoV-2) (Moore i Klasse 2020). Stoga su se različite farmaceutske tvrtke i istraživački timovi diljem svijeta natjecali u predstavljanju sigurnog i učinkovitog cjepiva protiv COVID-19 za upotrebu u međunarodnoj zajednici. Ovi napori su razvili druge platforme cjepiva za ulazak u pretklinička i klinička ispitivanja, a neka od njih su odobrena (Chen et al. 2021), uključujući tradicionalna cjepiva kao što su živa ili inaktivirana, podjedinična i cjepiva na bazi nukleinske kiseline kao cjepiva sljedeće generacije (Moore i Klasse 2020). Na temelju znanstvenih dokaza, živa oslabljena cjepiva stimuliraju urođeni, stanični i humoralni imunološki odgovor inducirajući Toll-like receptore (TLR) s dugotrajnim imunitetom i mogu razviti preosjetljivost. Glavni nedostatak ovih cjepiva je njihova skupa procjena sigurnosti i učinkovitosti. Inaktivirana virusna cjepiva slabo izazivaju stanične imunološke odgovore što umanjuje njihovu učinkovitost. U travnju 2020. inaktivirano cjepivo protiv COVID-19 proizveli su Sinovac i Wuhan Institute of Biological Products (Sinopharm) (Moore i Klasse 2020; Su et al. 2020). Podjedinična cjepiva su sigurna, s nekim nedostacima uključujući nisku imunogenost, potrebu za docjepljivanjem ili adjuvansom te visoku cijenu (Koirala i sur. 2020; Su i sur. 2020). Cjepiva na bazi nukleinskih kiselina razvijena su na temelju informacija o sekvencama. Oni uključuju DNA ili mRNA sekvence antigena koji snažno stimuliraju stanične i humoralne imunološke odgovore u različitim dozama. Zbog svojih prednosti, poput brze proizvodnje i najranijih cjepiva protiv COVID-19 u kliničkim ispitivanjima, uočljiva prednost cjepiva na bazi DNK njihova je stabilnost u različitim uvjetima skladištenja (Silveira et al. 2020; van Riel i de pamet 2020). Cjepiva na bazi RNA dobila su više pozornosti farmaceutskih tvrtki poput Pfizera/Biotecha i Moderne. Za razliku od DNA cjepiva, ona stimuliraju učinkovit humoralni imunološki odgovor kao TLR ligandi bez adjuvansa, a njihova je sekvenca modificirana kako bi spriječila degradaciju mRNA (Moore i Klasse 2020; van Riel i de Wit 2020; Soiza et al. 2021). Ovaj pregled imao je za cilj procijeniti nedavni razvoj cjepiva na bazi nukleinske kiseline, uključujući mRNA i DNA cjepiva protiv COVID-a-19.
Glavni tekst
Koronavirusni molekularni mehanizam infekcije i imunološki odgovor

biljka cistanche koja jača imunološki sustav
COVID{0}} genom je pozitivna jednolančana RNA koja kodira četiri glavna strukturna proteina koja se sastoje od ovojnice (E), šiljka (S), membrane (M) i nukleokapsida (N) (Stadler i Rappuoli 2005.), kao što je prikazano na slici 1a. Ljudski SARS-CoV obuhvaća šiljak (S) glikoprotein kao dio ovojnice. Inkorporaciju virusa u stanice domaćina izvodi spike protein koji se sastoji od S1 i S2 podjedinica. Oni igraju ključnu ulogu u vezivanju za receptore stanice domaćina poznate kao angiotenzin-konvertirajući enzim II (ACE2) za inicijaciju infekcije (slika 1b). Središnja regija S1 domene koja se veže na ACE2 s visokim afinitetom je receptor-vezujuća domena (RBD). U tom pogledu, interakcija između RBD-a i ACE2 potrebna je za inicijaciju infekcije ljudskih stanica (He et al. 2020). Osim toga, skraćivanje S proteina bitno je za ulazak virusa u stanice domaćina; nakon pričvršćivanja RBD regije na ACE2, proteaza domaćina poznata kao TM proteaza serin 2 (TMPRSS2) cijepa S protein na S1 i S2 domene što dovodi do fuzije S2 domene na stanicu domaćina (Huang et al. 2020). Iako su snažni imunološki odgovori učinkoviti protiv COVID-19, preosjetljivosti i citokinske oluje (uglavnom interleukina-6-, IL-1b, GM-CSF-, interferona- / IFN-, faktora nekroze / TNF -, IL-10-, IL-2- i IL- 7-potaknuti odgovori) moraju biti zabranjeni (Chowdhury et al. 2020). Nakon vezivanja virusa (interakcija šiljak-ACE2) i ulaska u respiratorne stanice, fagocitni alveolarni makrofagi i dendritične stanice (DC) predstavljaju virusne antigene T stanicama i aktiviraju T CD4+(pomoćne T stanice) i T CD{{37 }} (citotoksična T stanica). Potom se oslobađaju proupalni citokini poput IL6, IL12, TNF i IFN itd. kako bi se susreli s virusom. Međutim, visoke razine proizvodnje citokina koje dovode do citokinske oluje uzrokuju oštećenje pluća (Hosseini et al. 2020.). Prema znanstvenim dokazima, T-stanice pomoćnice neophodne su za eliminaciju virusne infekcije, indukciju B-stanica da proizvode protutijela i stimulaciju citotoksičnih T-stanica (Sharma et al. 2020.). Antigenski ciljevi za COVID‑19 U razvoju sigurnog i zaštitnog cjepiva protiv patogenog organizma ključno je identificirati najbolje imunogene ciljeve (Lu et al. 2020b). Usvajanje potencijalnih antigenskih ciljeva ključno je za provociranje T-staničnih i B-staničnih epitopa da pravilno induciraju staničnu i humoralnu imunost (Rueckert i Guzmán 2012). Virusni S protein stupa u interakciju sa stanicama domaćina preko RBD domene kao esencijalni ligand. RBD domena može potaknuti proizvodnju neutralizirajućih antitijela i T-stanični imunološki odgovor protiv COVID-a-19. Također, potvrđena je imunogenost S proteina (Pushparajah et al. 2021). N protein ima malu i visoko očuvanu sekvencu u usporedbi s drugim virusnim proteinima. Protein N je jako izražen tijekom infekcije virusom, sa značajnim povezanim humoralnim imunološkim odgovorom protiv COVID-19 među pacijentima. Uz to, uz stanični odgovor na N protein, može se smatrati odgovarajućim antigenom kandidatom u dizajnu cjepiva (Dutta et al. 2020.). Osim toga, M protein i E protein stimuliraju T CD4+epitope (Wang i sur. 2005; Abdelmageed i sur. 2020; Dong i sur. 2020). Izazivanje snažnih imunoloških odgovora protiv S proteina je odlučujuće i neophodno (Buchholz et al. 2004). S protein uključuje najimunogenije epitope T stanica i B stanica poznate kao preferirane mete u razvoju cjepiva protiv COVID-a-19. Primijenjeno je u svim razvijenim cjepivima mRNA platforme poput cjepiva Pfizer/BioNtech i Moderna.

Slika 1 a Struktura viriona SARS-CoV-2; glavni površinski proteini virusa COVID-19 uključuju Spike (S) glikoprotein, membranske (M) i proteine ovojnice (E). S protein je glavno cjepivo i terapeutski cilj koji stupa u interakciju s receptorom angiotenzin-konvertirajućeg enzima II (ACE2) za inicijaciju infekcije. b Domene spike proteina; S protein uključuje S1 (NTD ili neprevedenu domenu i RBD ili receptorsku veznu domenu) i S2 podjedinice
Povijest lijekova na bazi nukleinskih kiselina
Oligonukleotidi su ušli u klinička ispitivanja prije više od 30 godina. Povijest korištenja terapijskih pristupa temeljenih na nukleinskim kiselinama datira iz 1977. godine kada su Paterson i sur. koristili nukleinske kiseline za usklađivanje ekspresije gena (Paterson et al. 1977). Trenutno su dobili više pažnje. Lijekovi na bazi nukleinske kiseline podijeljeni su u različite kategorije, uključujući antisens oblike, ribozime, mRNA i cjepiva na bazi DNK (Sharma et al. 2014). Sintetski oligodeoksinukleotid inhibirao je replikaciju virusa Rousovog sarkoma (RSV), koji je bio komplementaran RSV mRNA i bio je poznat kao antisense (Zamecnik i Stephenson 1978). Prvi antisense uveden je u kliniku protiv citomegalovirusa (CMV) (Mulamba et al. 1998). Mala interferirajuća RNA (siRNA) posjeduje potencijal inhibicije ekspresije gena i prvi put je prijavljena 1998. Druga skupina malih nekodirajućih RNA uključuje mikroRNA (miRNA) koje imaju nezamjenjivu ulogu u regulaciji ekspresije gena, s funkcije slične onima siRNA i terapeutski potencijal (Usman i Blatt 2000; Sharma et al. 2014). Kao što je spomenuto, ribozimska klasa RNA molekula djeluje kao enzim koji cilja transkripciju. Ribozimi su ušli u klinička ispitivanja protiv raka i nekih virusnih infekcija kao što je virus humane imunodeficijencije (HIV) (Usman i Blatt 2000; Abera et al. 2012). Uz cjepiva koja se temelje na mRNA i DNA, ona se svrstavaju u lijekove na bazi nukleinske kiseline koji su uvedeni 1990. i dobili su više pažnje u razvoju cjepiva za borbu protiv COVID-a-19 (Le et al. 2020; Zhang et al. 2020). Glavne prednosti ovih skupina cjepiva uključuju njihovu brzu proizvodnju i visoku specifičnost protiv odgovarajućih ciljnih antigena (Le et al. 2020).

cistanche tubulosa-poboljšava imunološki sustav
mRNA‑ cjepiva
Početna isporuka molekula mRNA u stanice domaćina uključivala je transfekciju mRNA u stanice fibroblasta pomoću kationskog lipida (Park et al. 2021). mRNA cjepiva uključuju mRNA patogenih antigena koji ljudske stanice proizvode antigene proteine. Nekoliko prednosti mRNA cjepiva uključuje jednostavan proizvodni proces, učinkovit i zaštitni imunitet, prikladnu manipulaciju i industrijalizaciju te fleksibilnost u odgovoru na varijante COVID-19 (Kaufman et al. 2016; Fang et al. 2022). Neki pristupi, poput dodavanja 5'-cap i Kozak sekvenci, primjenjuju se pomoću 3'-poli-A sekvenci i modifikacije mRNA nukleozida (Borah et al. 2021). MRNA cjepiva se prevode u citosol domaćina. Stoga ne postoji rizik od umetanja genoma domaćina, što je poznato kao njihova glavna prednost. U tom smislu, cjepiva na bazi mRNA nedavno su dobila više pozornosti kao siguran preventivni pristup protiv raka i zaraznih bolesti (Kaur i Gupta 2020). Primarni mehanizam djelovanja mRNA cjepiva prikazan je na slici 2.
cjepiva na bazi DNK
DNA cjepiva sadrže nekoliko gena koji kodiraju virusne antigene peptide eksprimirane plazmidnim vektorima i prenošene u stanice putem elektroporacije (EP). U usporedbi s drugim platformama cjepiva, DNK cjepiva predlažu fleksibilnu i brzu platformu za razvoj cjepiva, što ih čini fascinantnom tehnologijom za borbu protiv epidemija u razvoju kao što je COVID-19. Štoviše, proizvodnja antigena DNK cjepiva događa se u ciljnim stanicama, što pomaže u rekapitulaciji prirodne konformacije virusnog antigena i post-translacijske modifikacije. Glavni nedostatak DNA cjepiva je njihova ograničena imunogenost. Stoga je važno razmotriti strategije kao što su adjuvans ili upotreba režima primarnog pojačanja koji bi mogao povećati potencijal DNK cjepiva. Također, integracija nukleinske kiseline u DNK domaćina još je jedan problem biološke sigurnosti koji rezultira onkogenezom i mutagenezom (Rauch et al. 2018). Iako je prema prijašnjim studijama rizik od umetanja DNA cjepiva zanemariv, WHO i FDA preporučuju primjenu sigurnosti DNA cjepiva za integraciju (Wang et al. 2004; Schalk et al. 2006). DNK cjepiva prenose gene koronavirusa u ljudske stanice. Princip cijepljenja ovisi o isporuci DNA u jezgru stanice tako da se započne transkripcija antigena i nakon nje slijedi translacija. DNA cjepiva obično koriste plazmide kao vektore. Ovisno o načinu primjene cjepiva, djeluju i na miocite i na keratinocite. Međutim, stanice koje predstavljaju antigen u blizini mjesta ubrizgavanja također se mogu izravno transficirati pomoću DNK cjepiva. U takvim slučajevima, proces unakrsnog primanja predstavlja antigene koji koriste obje molekule glavnog histokompatibilnog kompleksa (MHC-I/II) (Hobernik i Bros 2018). Generirani antigeni se oslobađaju pomoću apoptotičkih tijela ili egzosoma što rezultira njihovim prepoznavanjem od strane stanica koje predstavljaju antigen, što zauzvrat izaziva stanične i humoralne imunološke odgovore. Za stvaranje snažnog imunološkog odgovora koriste se različite strategije isporuke (Donnelly i sur. 2005; Li i Petrovsky 2016; Strizova i sur. 2021). Što se tiče imunološke regulacije tijekom infekcije COVID-19, otkriveno je da pacijenti s rizikom od perikardijalnog izljeva s pogrešnom prognozom ukazuju na povišen CD3+CD8+ T stanica plus smanjen CD{{ 18}}HLA-DR i T regulatorne (Treg) stanice (Duerr et al. 2020). Ovi rezultati pokazuju da do teške infekcije dolazi zbog neuravnoteženog imunološkog odgovora koji pogoršava bolesna stanja (Tay et al. 2020.). Napredak cjepiva protiv COVID-19 usmjeren je na razvoj učinkovitog i odgovarajućeg imunološkog odgovora (uključujući obje ruke) bez napretka u takvoj neravnoteži (Hobernik i Bros 2018). Iako su klinička ispitivanja DNA cjepiva na ljudima pokrenula potpune odgovore, ti su odgovori često neadekvatni da potaknu prihvatljive kliničke prednosti. Dodatno, osnovne komponente plazmidne DNA, na primjer, nemetilirane CpG sekvence, mogu uzrokovati aktivaciju urođenih imunoloških odgovora, povećavajući adaptivne imunološke odgovore protiv eksprimiranih antigena. Stoga su DNA cjepiva primjenjivija u veterini (Coban i sur. 2013; Silveira i sur. 2017; Hobernik i Bros 2018). Zbog ovog nedostatka, neki pravci istraživanja koncentriraju se na optimizaciju i isporuku DNA cjepiva, uključujući optimizaciju kodona, dizajn promotora, molekularne adjuvanse, primjenu EP-a, cijepljenje s primarnim pojačanjem ili metode "omics" za napredni dizajn cjepiva (Li et al. 2012.; Silveira i dr. 2020.). Slika 3 ilustrira glavne faze mehanizama DNA cjepiva u učinkovitim imunološkim odgovorima.
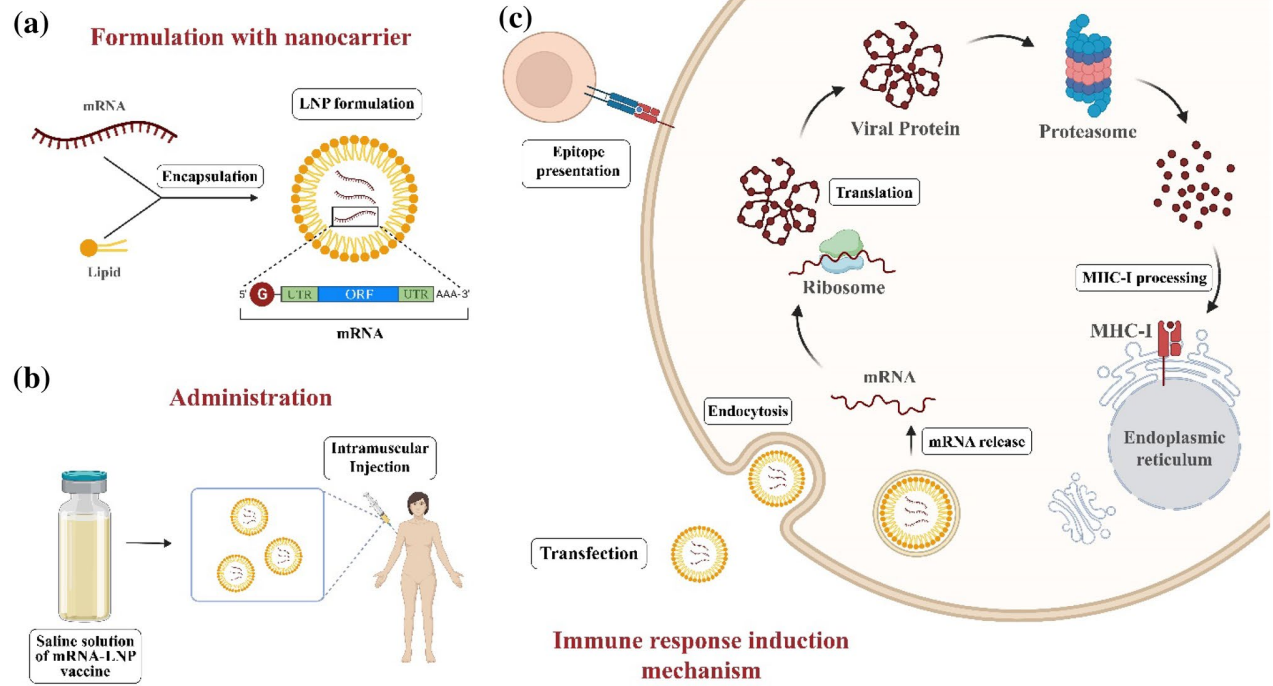
Slika 2 Formulacija mRNA cjepiva, primjena i mehanizmi imunološke provokacije: formulacija mRNA s lipidnim nanočesticama (LNP) održava i poboljšava stabilnost sekvence. b Slana otopina cjepiva mRNA-LNP primjenjuje se intramuskularnim putem. c MRNA koja sadrži LNP transfektira se u stanice koje predstavljaju antigen (APC) kroz endocitozu. MRNA se oslobađa u citoplazmi i prevodi u virusne proteine, zatim ih lizira proteasom i vežu se na glavni histokompatibilni kompleks I (MHC-I) na površini endoplazmatskog retikuluma i prezentiraju T citotoksičnim (Tc) stanicama
Potencijal cjepiva na bazi mRNA- i DNA
Struktura cjepiva na razini mRNA sadrži elemente za poboljšanje stabilnosti i ekspresije proteina, uključujući 3' UTR, kodirajuću sekvencu, 5'UTR, 5' kapu i poli (A) rep (Liu 2019). 5' i 3' UTR elementi koji okružuju kodirajuću sekvencu izvedenu iz virusnih ili eukariotskih gena poboljšavaju strukturnu stabilnost i poboljšavaju translaciju mRNA što su ključni čimbenici za cjepiva (Ross i Sullivan 1985; Holtkamp et al. 2006). Za učinkovitu translaciju proteina iz mRNA, potrebna je 5' cap struktura (Martin et al. 1975; Ross i Sullivan 1985). Rep mRNA poli (A) također ima regulatornu ulogu u stabilnosti i translaciji mRNA (Holtkamp et al. 2006). Također, upotreba kodona ima vitalnu ulogu u translaciji proteina. U tom smislu, kako bi se povećala translacija proteina iz mRNA, rijetki kodoni se zamjenjuju korištenim sinonimnim kodonima koji imaju obilje srodne tRNA u citosolu (Stepinski et al. 2001). Drugi pristup optimizaciji slijeda je obogaćivanje G:C sadržaja. Nekoliko je metoda posljednjih godina razvilo učinkovita i sigurna kandidatska DNK cjepiva. U platformi cjepiva temeljenoj na DNK, plazmidni vektori izvedeni iz bakterija primjenjuju se za ekspresiju željenih antigena unutar stanica domaćina. Bakterijski plazmidi moraju se unijeti u eukariotske stanice i premjestiti u jezgru. DNK se zatim transkribira i prevodi sa stranih gena u jezgri stanice domaćina, odnosno citoplazmi. Stoga je dizajniranje odgovarajućeg plazmida s visokom učinkovitošću transfekcije i ekspresije proteina ključno za postizanje snažnog DNA cjepiva (Malone et al. 1989). Sekvenca eukariotske regije (u plazmidima DNA cjepiva), uzvodno od umetnutog gena, sastoji se od promotora i poli A signala (poliA) (AAU AAA) koji se nalazi na 3' krajevima antigenske sekvence (Shan et al. 2011). Promotori su ključni elementi potrebni u plazmidima DNA cjepiva za izazivanje visokih razina ekspresije željenih antigena u stanicama domaćina (Becker et al. 2008) i rezultiraju transkripcijom mRNA iz umetnutog gena. Najčešće korišteni promotor u DNA cjepivima uključuje promotor humanog citomegalovirusa (CMV). Signal poliA sekvence uzrokuje stabilnost i prijenos mRNA i učinkovitu ekspresiju eukariotskog gena. Drugi kritični element je Kozakova sekvenca (ACCATGG) koja ima vitalnu ulogu u prevođenju pomoću eukariotskog ribosoma. Također, dodavanje jednog ili dva slijeda stop-kodona potrebno je kako bi se izbjegla netočna translacija umetnutog gena u stanicu domaćina (Becker et al. 2008; Williams 2013). Usporedba platformi DNA i mRNA cjepiva Iako su DNA i mRNA cjepiva u razvoju od 1990-ih i nedavnog razvoja i licenciranja raznih veterinarskih DNK cjepiva, značajan entuzijazam okrenuo se mRNA. Objema su potrebni napori da se poboljša njihova antigenost, stabilnost i učinkovitost izravnom manipulacijom plazmidne DNA i mRNA ili dodavanjem imunomodulatora ili adjuvansa te formulacija i sustava za isporuku (Liu 2019.). Trajanje stabilnosti mRNA je niže nego kod plazmidne DNA. Otkriveno je da DNA cjepiva brzo stvaraju kodirani protein, što je veća količina nego mRNA cjepiva zbog veće unutarnje stabilnosti plazmidne DNA. Utvrđeno je da plazmidna DNA postoji u mišićima do 6 mjeseci u neintegriranom načinu (Ledwith et al. 2000). Iako bi DNA i mRNA cjepiva trebala biti sustav ekspresije za omiljeni protein, nijedno nije imunološki inertno. Također, DNA plazmidi kao i mRNA stimuliraju urođeni imunitet (Campbell 2017). Tehnologija cjepiva temeljena na DNA i mRNA možda nije posve općenita. mRNA je kompliciranija od plazmidne DNA zbog modificiranih nukleozida i formulacija potrebnih za isporuku, stabilnost i nužnosti kontrole intrinzične imunostimulacijske aktivnosti mRNA. Ipak, koristi proizvodnji koja izbjegava potražnju za svakim staničnim ili životinjskim proizvodom. Obećanje je da će klinička postignuća biti izvediva nakon što se izazovi plazmidske DNK i mRNA cjepiva riješe posebno primjenom naprednih tehnologija za prevenciju i liječenje bolesti (Liu 2019.).

Slika 3. Proces ekspresije DNA cjepiva protiv COVID-19 u stanice koje predstavljaju antigen (dendritičke stanice ili DC). Plazmidna DNA ulazi u DC jezgru i eksprimira antigene in vivo (1) Zatim se antigeni prezentiraju T stanicama (T stanični receptori ili TCRs) preko MHC-I i MHC-II molekula. Predstavljanje antigena događa se putem DC CD80/86 molekula i CD8+T stanica CD28 molekula uz MHC-I-TCR i također putem DC CD40 i CD4+T stanica CD40L uz Interakcije MHC-II-TCR (2a, 3 i 4) Aktivacija i proliferacija CD8+T stanica i oslobađanje citokina dovodi do učinkovitih imunoloških odgovora kao što je aktivacija makrofaga (2b) Dodatno, aktivacija CD-a 4+T stanice nakon vezanja i učinaka citokina iz DC-a povezane su s aktivacijom B stanica, proliferacijom i lučenjem protutijela (5)
Napredak u isporuci cjepiva DNA i mRNA
Unos strane DNA i RNA od strane eukariotskih stanica nije učinkovit u usporedbi s virusnim vektorima. Utvrđeni su mnogi pristupi fizičkoj isporuci kako bi se povećao kapacitet staničnog unosa (Mellott et al. 2013.). Fizičke metode transfekcije gena uključuju sustave isporuke koji prenose genetski materijal putem mehaničkih postupaka, uključujući EP i projektorske uređaje (Gulce-Iz i Saglam-Metiner 2019). Uređaji Biojector koriste tlak CO2 za prijenos terapeutika kroz IM (intramuskularno), ID (intradermalno) i također SC (subkutano) davanje bez potrebe za iglom (Jorritsma et al. 2016.), dajući značajne prednosti u odnosu na konvencionalno ubrizgavanje iglom, uključujući ublažavanje štetni učinci, unakrsna kontaminacija iglom i oštećenja od uboda iglom (Zhang et al. 2015.). Relevantno, dva DNA cjepiva procijenjena su protiv virusa Zika u ispitivanju faze I, pokazujući povećane stanične odgovore nakon primjene bez igle u usporedbi s uporabom igle (Gaudinski et al. 2018.). Štoviše, platforma za isporuku mRNA cjepiva protiv bjesnoće koja koristi projektor otkrila je pojačane odgovore protutijela (Alberer et al. 2017.). Povećana učinkovitost cjepiva kroz mlaznu injekciju može se pripisati široj distribuciji cjepiva, što rezultira većim unosom pomoću APC-a (Williams et al. 2000; Alberer et al. 2017). Trenutačno se za isporuku DNA cjepiva u kliničkim studijama obično koriste ID ili IM injekcije nakon kojih slijedi EP (Sardesai i Weiner 2011). EP uključuje stvaranje pora unutar stanica kože kako bi se povećao stanični unos genetskog materijala pomoću električnih impulsa (Pushparajah et al. 2021.). Metoda IM EP prvenstveno je primijenjena 1998. (Aihara 1998.) povećavajući propusnost mišićnih stanica za isporuku DNK cjepiva (Rizzuto i sur. 1999.; Dupuis i sur. 2000.; Sokołowska i Błachnio-Zabielska 2019.). Brojna su izvješća otkrila bolju ekspresiju antigena i povećane antigen-specifične imunološke odgovore in vivo korištenjem EP (Yan i sur. 2008; Yan i sur. 2009). Zabilježeno je da je HIV DNA cjepivo, ADVAX, povećalo imunogenost nakon prijenosa kroz EP (Vasan et al. 2011.), u usporedbi s IM primjenom (Vasan et al. 2010.). Unatoč tome, EP pristup pati od rizika od smrti stanica zbog korištenja visokih napona (Gulce-Iz i Saglam-Metiner 2019.). Novi pristupi isporuci, kao što je EP, još se istražuju za isporuku RNA cjepiva.

koristi cistanche za muškarce-jača imunološki sustav
Učinkovitost EP za isporuku cjepiva koja se samo pojačavaju bila je slična onoj za cjepiva s plazmidnom DNA u smislu ekspresije gena i imunoloških odgovora kod miševa (Cu et al. 2013). Međutim, EP nije poboljšao učinkovitost isporuke tradicionalnih nereplicirajućih RNA cjepiva (Johansson et al. 2012.), što je moguće smanjilo njihovu učinkovitost u dupliciranju RNA vektora. U skladu s tim, EP i bio injektori imaju prednost za parenteralnu injekciju COVID-19 DNA/RNA cjepiva. Ovi pristupi pridonose većoj proizvodnji i isporuci kandidata za DNK cjepivo i značajno poboljšavaju rezultate (Pushparajah et al. 2021.).
Prednosti i ograničenja cjepiva na bazi nukleinske kiseline
Kao nove i obećavajuće metode imunizacije, cjepiva na bazi nukleinske kiseline pružaju uvid u razvoj sigurnog i zaštitnog cijepljenja (Choi i Chang 2013.) kao što su pokazali milijuni ljudi tijekom pandemije COVID-19. Cjepiva na bazi nukleinske kiseline imaju kratke razvojne cikluse, što omogućuje brzu distribuciju tijekom pandemije. Korištenje rekombinantnih DNA cjepiva zahtijeva učinkovit prijenos DNA vektora u jezgru, transkripciju i potom translaciju u željeni antigen (Leitner et al. 1999). Zbog prikladne manipulacije i jeftine proizvodnje, goli plazmidni DNK je fascinantan vektor za prezentiranje antigena (Williams 2013). Obično se plazmidna DNA sastoji od osnovnih genetskih elemenata, uključujući gen koji kodira antigen, promotor, pojačivače i sekvence završetka transkripcije/poliadenilacije (Vogel i Sarver 1995.). Platforma plazmidne DNK obećavajući je biofarmaceutski konstrukt koji se replicira u visokim razinama unutar jeftinih prokariotskih stanica iako zahtijeva pročišćavanje (Prazeres et al. 1999; Ferreira et al. 2000; Suschak et al. 2017). RNA cjepiva sastavljena su od mRNA molekula koje sadrže antigen RNA okružen 3', poli-A repom i 5' krajevima i nemaju zahtjev za transkripciju. (Zhang i dr. 2019.). Nekoliko RNA cjepiva prolazi kroz samopojačavanje poznato kao nova tehnologija u razvoju. Sukladno tome, molekula RNA može se replicirati i prevesti u domaćinu nakon isporuke, unatoč mogućnosti gole nestabilnosti RNA, čime se povećava ekspresija imunogenih peptida (Pardi i sur. 2018; Zhang i sur. 2019; Wadhwa i sur. 2020) . MRNA se razgrađuje sveprisutnim enzimima ribonukleazom (Wadhwa et al. 2020; Xu et al. 2020). Dodatak 3' poli-A repa i 5'–7-metilgvanozinski poklopac je kritičan za povećanje stabilnosti i translacije mRNA u citosolu (Gallie 1991; Schlake et al. 2012). Strategije za povećanje unosa i ekspresije cjepiva uglavnom su procijenjene za DNA cjepiva nego za RNA cjepiva, budući da DNA zahtijeva prolazak kroz dvije stanične membrane da bi dosegla jezgru. Nasuprot tome, RNA prodire u citoplazmu kroz jednu membranu (Rauch et al. 2018). Struktura DNK ima relativno veću stabilnost. Tijekom 7 godina utvrđeno je da je plazmidna DNK ostala netaknuta bez razlike s novonabavljenom DNK koja je držana na -20 stupnjeva (Walther et al. 2013; Pushparajah et al. 2021). Nizak pH i temperatura ključni su za dugotrajno održavanje integriteta DNK. Nasuprot tome, RNA je iznimno osjetljiva na temperaturu i mora se držati na -70 stupnjeva u mediju bez enzima kako bi se produžio njezin poluživot (Jones et al. 2007).
Izazovi u razvoju cjepiva na bazi nukleinske kiseline
Dobro je poznato da cjepiva protiv COVID-a-19 moraju biti učinkovita i dovoljno zaštitna (Graham 2020.) i izazvati dugotrajni imunitet. Međutim, godišnje cijepljenje može biti moguće na temelju godišnjeg iskustva s cjepivom protiv gripe (Randolph i Barreiro 2020; van Riel i de Wit 2020). Razvoj cjepiva protiv COVID-19 postavlja izazove čak i s novim platformama. Unatoč visokoj imunogenosti i zaštiti proteinskog cjepiva protiv koronavirusa, pojava mutacija izaziva zabrinutost i ponovnu pojavu virusa. Stoga je prognoza vremena i mjesta pojave bolesti zajedno s točnim usvajanjem sekvence ciljnog proteina prva faza razvojnog procesa koja zahtijeva pravilnu provedbu kliničkih ispitivanja (Lurie et al. 2020.). Glavni izazov DNK cjepiva je izazivanje relativno nižih imunoloških odgovora kod ljudi i velikih životinja nego kod malih životinjskih sustava (Grunwald i Ulbert 2015; Suschak et al. 2017). Primjetno je da i dalje treba rješavati daljnje izazove u vezi s cjepivima protiv COVID-19 kao što su trajnost zaštite, učinkovitost u određenim podskupinama, sprječavanje prijenosa virusa i javno prihvaćanje (Pushparajah et al. 2021.). Odgođena ekspresija antigena u samopojačavajućim mRNA cjepivima može ograničiti učinkovitost ovih cjepiva. Međutim, ova platforma daje veće prinose i stoga pruža ekvivalentnu zaštitu pri znatno nižim dozama (Vogel et al. 2018; Strizova et al. 2021).
Nedavni napredak u DNK i mRNK cjepivima protiv COVID‑19
U razvoju cjepiva protiv COVID-a{{0}}, brojne su se studije usredotočile na platforme cjepiva mRNA (Verbeke et al. 2021) što je dovelo do odobrenja nekoliko cjepiva (Vitiello i Ferrara 2{{ 94}}21) poput onih iz tvrtki Moderna i Pfizer/BioNtech. Cjepivo Moderna uključuje cjelokupno kodiranje COVID-19 spike glikoproteinske mRNA, dok Pfizer/BioNtech sadrži RBD mRNA sekvencu (Brüssow 2020). Razine učinkovitosti cjepiva Pfizer/BioNTech i Moderna uključuju 95% odnosno 94,5% (Rauch i sur. 2021.; Widge i sur. 2021.). Temperatura skladištenja cjepiva Moderna je između -25 stupnjeva i -15 stupnjeva, dok je temperatura skladištenja cjepiva Pfzer između -80 stupnjeva i -60 stupnjeva (Meo et al. 2021; Rauch et al. 2021). U usporedbi s cjepivom Moderna, cjepivo Pfizer/BioNTech ima niže troškove i nuspojave (Rauch et al. 2021). Drugo mRNA cjepivo protiv COVID-19 razvili su kineski istraživači i koristilo je termostabilnu (najmanje tjedan dana na 25 stupnjeva) mRNA koja kodira RBD (Brüssow 2020.). U drugom istraživanju, CureVac je korišten kao projektirana platforma mRNA S proteina pune duljine za razvoj cjepiva protiv COVID-19 sa zamjenama u dva prolinska ostatka za poboljšanje stabilnosti proteina (Rauch et al. 2021). Ruklanthi de Alwis i sur. (2021.) razvili su samotranskripcijsko i replicirajuće mRNA cjepivo za COVID-19 koristeći S protein pune duljine i replikon (de Alwis et al. 2021.) s potencijalom primjene kao učinkovito i sigurno cjepivo s jednom dozom za borbu protiv COVID-a- 19 (de Alwis et al. 2021.). Slično tome, korištena je samopojačavajuća RNK koja kodira COVID-19 S protein inkapsulirana unutar lipidne nanočestice (LNP) i ukazala je na visoke titre antitijela i staničnih imunoloških odgovora (McKay et al. 2020.). Za SARS-CoV razvijeni su neki kandidati za DNK cjepivo, kao što su cjepiva na bazi proteina S, N i M. Među njima, DNA cjepivo na bazi S proteina učinkovito je izazvalo zaštitni učinak protiv infekcije COVID-19, vjerojatno zahvaljujući vitalnoj ulozi S proteina u vezivanju receptora (Zhao et al. 2020.). INO-4800 je kandidat za DNK cjepivo protiv COVID-19 koji kodira COVID-19 S protein (Sarwar et al. 2020; Smith et al. 2020). Pretklinički rezultati kod miševa i zamoraca pokazali su humoralni i stanični imunološki odgovor. U kliničkim studijama faze I, dvije doze INO-4800 ubrizgane su putem ID puta, nadopunjene EP-om putem CELLECTRA®2000 Inovio Pharmaceutical (Diehl et al. 2013; Amante et al. 2015). Potpuni imunološki odgovor objašnjen je na temelju antitijela i staničnih odgovora kod 34 od 36 sudionika u njihovoj fazi I kliničkog ispitivanja. Uočeno je deset prijavljenih nuspojava (AE) bez ozbiljnih nuspojava (SAE) (faza). Pokrenuto je kliničko ispitivanje faze I/II za procjenu imunogenosti, sigurnosti i podnošljivosti INO- 4800 (Tebas et al. 2019.). INO-4800 ima slične uvjete skladištenja (Smith et al. 2020), u nadi za jednostavniju distribuciju cjepiva. Osim toga, neke druge grupe DNK cjepiva protiv COVID-a-19 pokrenule su ispitivanja. U lipnju 2020. kliničko ispitivanje faze I i IIa za GX-19 pokrenulo je zapošljavanje. DNK cjepivo, AG0301-COVID-19, proizvedeno zajedničkim pokušajima Sveučilišta Osaka (Japan), Takaro Bio i AnGes, pokrenulo je zapošljavanje za klinička ispitivanja faze I i II u srpnju 2020. za procjenu njegovu imunogenost i sigurnost (Speiser i Bachmann 2020). Provedena su klinička ispitivanja faze I i II za procjenu imunogenosti i sigurnosti tri doze ZyCoV-D (Kumar et al. 2021). Ovo oralno cjepivo kodiralo je šiljasti protein u plazmidnoj DNA, dinamički pojačan u živoj Bifidobacterium longum, dobro poznatoj crijevnoj probiotičkoj bakteriji. Pokrenuto je drugo kliničko ispitivanje faze I za procjenu CORVax12, DNK cjepiva koje kodira spike protein. Ispitivana je učinkovitost elektroporiranog CORVax12 samog ili u kombinaciji s drugim plazmidom koji kodira interleukin 12 (IL-12). Razna mRNA cjepiva protiv COVID-19 su u razvoju i pokazala su obećavajuće rezultate (Leitner i sur. 1999; Croyle i sur. 2001). Raznovrsni pristup razvoju RQ3013-VLP (koji kodira proteine S, E i M) bio je učinkovit in vivo korištenjem koktela mRNA. Ovo mRNA cjepivo integrirano je s promijenjenim nukleozidima, a zatim upakirano u LNP i razotkrilo sposobnost izazivanja jakih staničnih i humoralnih imunoloških odgovora kod miševa (Le et al. 2020; Lu et al. 2020a). Projektirano DNK cjepivo s domenom arginil-glicil-asparaginske kiseline (RGD) u dvije doze od 60 µg korištenjem elektroporacije poboljšalo je učinke kod BALB/cJ miševa (Guo et al. 2021.). IM + jet injekcija DNA cjepiva u jednoj dozi (0,2 mg) mogla bi imunizirati sirijske hrčke (Brocato et al. 2021). Drugo DNK cjepivo koje koristi S protein podvrgnuto u tri doze zaštitilo je Rhesus macaque (Yadav et al. 2021). Fuzija RBD-a s preS1 amino-terminalom virusa hepatitisa B i IM injekcija za tri doze (tjedni 0, 2 i 4) kod C57BL/6 miševa izazvala je humoralni i stanični imunološki odgovor (Jeong et al. 2021). Dodatno, IM injekcija plazmidne DNA proteina S i podjedinice S1 (rekombinantni protein) u tri doze u tjednima 0, 2 i 8 kod Rhesus makakija stimulirala je neutralizirajuća protutijela (Prompetchara et al. 2021.). IM+EP injekcija S proteina u tri doze (tjedni 0, 2 i 4) kod ICR miševa stimulirala je humoralne i stanične odgovore (Li et al. 2021). Druga DNK cjepiva u kliničkim ispitivanjima uključila su S protein u fazama I/II u lipnju 2022. (NCT04445389, IM put kod odraslih u dobi od 18 do 50 godina), u srpnju 2021. (NCT04463472, IM put kod odraslih u dobi od 20 do 60 godina), Rujan 2021. (NCT04527081, IM put u odraslih od 20 do 65 godina) i faza I (NCT04336410, ID put u 18 godina i stariji), veljača 2022. (NCT04334980, oralno u odraslih s 18 godina i stariji) i lipanj 2021. ( NCT04591184, IM put u odraslih 18–84 godine). Osim toga, mRNA cjepiva u kliničkim ispitivanjima uključivala su ona u fazi II u studenom 2021. (NCT04515147, IM, 18-60 godina), fazi II-III u prosincu 2022. (NCT04368728, IM u odraslih 18-85 godina) i fazi I u lipnju 2021. (NCT04566276, IM u odraslih 18–75 godina). COVID-eVax bilo je cjepivo temeljeno na RBD-u koje je izazvalo dovoljan imunološki odgovor kod miševa, tvorova i štakora nakon 38 dana (Conforti et al. 2022.). Dva (X-19 i GX-19N) DNA cjepiva koja kodiraju proteine šiljaka i nukleokapsida procijenjena su u ispitivanjima faze I među odraslim osobama u dobi od 19 do 49 godina, a vezna protutijela mogla su se otkriti pri drugoj dozi cijepljenja. Potvrđena je sigurnost i podnošljivost ovih cjepiva, gdje je GX-19N inducirao više razine T stanica i odgovora protutijela (Ahn et al. 2022.). Xcl1-SARS-CoV-2 spike fuziono DNA cjepivo izazvalo je veću stopu odgovora posredovanih protutijelima i T stanicama u usporedbi s šiljastim genom koji sadrži plazmid pojedinačno in vitro i in vivo (Qi et al. 2022). Nedavno bakulovirusno COVID-19 Delta DNA cjepivo moglo bi zaštititi 100% miševa od COVID-a-19 (Jang et al. 2023.). Linearna DNA (linDNA) koja kodira SARS-CoV-2 RBD (Lin-COVIDeVax) uspjela je izazvati odgovore protutijela i T stanica te pružiti sigurnost i izostati štetne učinke (Conforti et al. 2023.). Tablica 1 predstavlja klinička ispitivanja i odobrena cjepiva protiv COVID-a na bazi nukleinske kiseline-19. Prema ažuriranim podacima, 229 820 324 osobe primile su cjepiva protiv COVID-19 širom svijeta, među kojima su one iz afričkih zemalja imale nižu stopu cijepljenja (https://www.usnews.com/news/coronavirus-and -vijesti o cjepivu, https://www.bloomberg.com/graph ics/covid-vaccine-tracker-global-distribution/). U skladu s tim, stopa cijepljenja povezana je s ekonomskim uvjetima različitih regija/područja.
Potencijalni sigurnosni problemi za cjepiva protiv COVID‑19
Praćenje sigurnosti u svakom razvijenom preventivnom ili profilaktičkom cjepivu jedan je od bitnih aspekata. Upotreba otrovnih kemikalija ili stanične kulture nije potrebna u procesima proizvodnje mRNA cjepiva, stoga je poznato kao sigurna platforma. Kratko vrijeme proizvodnje također smanjuje rizik od kontaminacije mikroorganizmima (Wang et al. 2020). Najčešće prijavljeni učinci uključuju glavobolju, umor i druge sistemske ozbiljne događaje, poput vrućice, zimice, mijalgije, povraćanja, bolova u trbuhu i rijetkih izvješća o proljevu. Međutim, nije primijećena smrt kod primatelja mRNA cjepiva (Chapin-Bardales et al. 2021; Skowronski i De Serres 2021). Neke sistemske nuspojave, poput anafilaksije, obično se prijavljuju kod pojedinaca s poviješću alergija i procjenjuju se na 2,5–11,1 slučajeva po milijun doza (Shimabukuro et al. 2021.). Snažan imunološki odgovor kod ljudi mlađih od ostalih može dovesti do visokih sistemskih događaja i više nuspojava je prijavljeno nakon ubrizgavanja druge doze cjepiva u usporedbi s prvom dozom (Male 2021; Skowronski i De Serres 2021). Osim toga, bol na mjestu ubrizgavanja, crvenilo i oteklina prijavljeni su kao najčešće lokalne nuspojave (Anand i Stahel 2021). Na temelju dostatnih dokaza odobrenih mRNA cjepiva, uključujući Pfizer/BioNTech i Modernu, nije dokazan rizik od pobačaja u trudnoći (stopa=0%) (Muški 2021.). Primjetno je da su DNA cjepiva dovoljno sigurna, ali nisu uvijek imunogena; stoga dovoljan imunološki odgovor zahtijeva dodatne doze. Humoralni imunološki odgovor nije bio dosljedan u ispitivanjima na ljudima, dok se čini da je stanični imunitet češći. Sukladno tome, sigurnost DNK cjepiva među starijom i mlađom populacijom je povoljnija (Ledgerwood i sur. 2011.; Houser i sur. 2018.; Carter i sur. 2019.). Sigurnosna zabrinutost ukazuje na moguću integraciju transfektirane DNA u germinalnu liniju i somatske stanice domaćina. U tim slučajevima, disregulacija ekspresije gena vjerojatno se javlja zajedno s višestrukim značajnim mutacijama. Ipak, samo ekstrakromosomski plazmidi i plazmidi s nedostatkom kromosomske integracije obično se koriste u razvoju DNA cjepiva. Osim toga, većina plazmida ostaje na mjestu primjene (Schalk et al. 2006). Nedavni sustavni pregled i meta-analiza pokazali su da su cjepiva mRNA povezana s većim brojem nuspojava u usporedbi s drugim platformama (Kouhpayeh i Ansari 2022.). Nedavno je primijećen rijedak slučaj miozitisa povezanog s cjepivom BNT162b2 mRNA kod 34-godišnje žene (Magen et al. 2022.). Metilacija DNA i odgovarajuće epigenetske promjene također ometaju učinkovitost DNA i mRNA cjepiva (Pang et al. 2022.). Primjetno je nekoliko odobrenih cjepiva nukleinskih kiselina (ZyCoV-D, DNA plazmidno cjepivo koje se koristi intradermalno, Indija), BNT162b2 (mRNA, 2 doze, Njemačka), mRNA- 1273 (Moderna, SAD, 2 doze), ARCoV (WALVAX, Kina) i klinička ispitivanja uključujući 302-COVID19 (DNA plazmidno cjepivo, faza II/III intramuskularno, Japan), INO-4800 (DNA plazmid, faza II/III, intradermalno, Kina), GX{{36 }}N (DNK cjepivo, Genexine, faza II/III), Covigenix VAX-001 (DNK cjepivo, Entos Pharmaceuticals, faza I/II, intramuskularno), COVID-eVax (DNK cjepivo, faza I/II, intramuskularno , Rim) i bacTRL-Spike (DNK cjepivo, faza I, oralno, Symvivo) su razvijeni (Sheridan 2021; Liu i Ye 2022a). Ova su cjepiva stimulirala humoralni i stanični imunitet osim protiv GX-19N i AG0302- COVID-19. Neki štetni učinci cjepiva na bazi nukleinske kiseline protiv COVID-19 uključuju bol, limfadenopatiju, eritem, crvenilo, oticanje, mučninu, umor, artralgiju, mialgiju, vrućicu, kardiorespiratorni arest, moždani udar, reakciju preosjetljivosti, alkoholnu bolest jetre, Bellovu paralizu , paroksizmalna ventrikularna aritmija i smrt (Norquist i sur. 2012; McNeil i DeStefano 2018; Baden i sur. 2021; Momin i sur. 2021; Liu i Ye 2022b, 2022a).
Feniletanol glikozid je glavna aktivna komponenta Cistanche deserticola
Zaključak
Brza pandemija COVID-a-19 stvorila je nezadovoljenu potrebu za razvojem učinkovitih cjepiva za sprječavanje bolesti. Iako je imunogenost DNK cjepiva kod životinja prihvatljiva, klinička validacija je opravdana kod ljudi. RNK cjepiva mogu pružiti odgovarajuća imunološka svojstva i značajne prednosti u odnosu na DNK cjepiva. Problemi s nestabilnom prirodom RNA riješeni su korištenjem odgovarajućih pristupa skladištenju i formulacija kako bi se zaustavila njezina razgradnja. Sigurnost cjepiva također je važna i ne može se ugroziti radi veće učinkovitosti. Postoje odobrena cjepiva na bazi nukleinske kiseline za kontrolu širenja COVID-19. Praćenje sudionika mora se nastaviti. Postoji potreba za učenjem o nuspojavama COVID-19 cjepiva temeljenog na nukleinskoj kiselini. Štoviše, ponovna procjena cjepiva i razvoj polivalentnih cjepiva ili pan-koronavirusnih strategija obećavaju s obzirom na ponovnu pojavu novih zabrinjavajućih varijanti.
Tablica 1. Klinička ispitivanja i odobrena cjepiva protiv COVID-19 bolesti i njihove karakteristike


Reference
Abdelmageed MI et al (2020.) Dizajn multiepitopskog peptidnog cjepiva protiv E proteina ljudskog COVID-a-19: imunoinformatički pristup. Int J Biomed Clin Anal. https://doi.org/ 10.1155/2020/2683286
Abera G, Berhanu G, Tekewe A (2012.) Ribozimi: enzimi nukleinske kiseline s potencijalnom farmaceutskom primjenom: pregled. Pharmacophore 3:164-178
Ahn JY et al (2022.) Sigurnost i imunogenost dvaju rekombinantnih DNK COVID-19 cjepiva koja sadrže kodirajuće regije šiljka ili šiljka i nukleokapsidnih proteina: privremena analiza dvaju otvorenih, nerandomiziranih ispitivanja faze 1 kod zdravih odraslih osoba. Lancetni mikrob 3:e173–e183. https://doi.org/10.1016/ S2666-5247(21)00358-X
Aihara H (1998) Miyazaki J. prijenos gena u mišić elektroporacijom in vivo. Nat Biotechnol 16:867–870. https://doi.org/10. 1038/nbt0998-867
Alberer M et al (2017.) Sigurnost i imunogenost mRNA cjepiva protiv bjesnoće u zdravih odraslih osoba: otvoreno, nerandomizirano, prospektivno kliničko ispitivanje prve faze na ljudima. The Lancet 390:1511-1520.https://doi.org/10.1016/s0140-6736(17)31665-3
Amante DH et al (2015.) Obrasci transfekcije kože i kinetika ekspresije isporuke plazmida poboljšane elektroporacijom pomoću CELLECTRA-3P, prijenosnog uređaja za dermalnu elektroporaciju sljedeće generacije. Metode humane genske terapije 26:134–146. https:// doi.org/10.1089/hgtb.2015.020
Anand P, Stahel VP (2021.) Pregledajte sigurnost Covid-19 mRNA cjepiva: pregled. Pacijent Saf Surg 15:20. https://doi.org/10.1186/ s13037-021-00291-9
Baden LR et al (2021.) Učinkovitost i sigurnost mRNA-1273 SARS CoV-2 cjepiva. N Engl J Med 384:403–416. https://doi.org/10. 1056/NEJMoa2035389
Becker PD, Noerder M, Guzmán CA (2008.) Genetska imunizacija: bakterije kao prijenosnici DNA cjepiva. Hum Vaccin 4:189-202.https://doi.org/10.4161/hv.4.3.6314
Borah P et al (2021.) Perspektive kandidata za RNA cjepivo za COVID-19. Front Mol Biosci. https://doi.org/10.3389/fmolb. 2021.635245
Brocato RL i suradnici (2021.) Zaštitna učinkovitost SARS-CoV-2 DNK cjepiva kod sirijskih hrčaka divljeg tipa i imunosuprimiranih. Npj cjepiva 6:1–7.https://doi.org/10.1038/s41541-020-00279-z
Brüssow H (2020.) Napori prema cjepivu protiv COVID-19. Environ Microbiol 22:4071-4084. https://doi.org/10.1111/1462-2920. 15225
Buchholz UJ et al (2004.) Doprinosi strukturnih proteina teškog akutnog respiratornog sindroma koronavirusa zaštitnom imunitetu. Proc Natl Acad Sci 101:9804-9809. https://doi.org/ 10.1073/pnas.0403492101
Campbell JD (2017) Razvoj CpG adjuvansa 1018: studija slučaja. Adjuv za cjepivo. https://doi.org/10.1007/ 978-1-4939-6445-1-2
Carter C et al (2019) Sigurnost i imunogenost ispitivanog sezonskog hemaglutininskog DNA cjepiva protiv infuence praćenog trovalentnim inaktiviranim cjepivom primijenjenim intradermalno ili intramuskularno u zdravih odraslih osoba: Otvoreno randomizirano kliničko ispitivanje faze 1. PLoS One 14:e0222178. https://doi.org/10.1371/journal.pone.0222178
Chapin-Bardales J, Gee J, Myers T (2021.) Reaktogenost nakon primitka cjepiva protiv COVID-19 temeljenih na mRNA. JAMA. https://doi. org/10.1001/jama.2021.5374
Chen Y, Cheng L, Lian R, Song Z, Tian J (2021.) Istraživanje cjepiva protiv COVID-19 usredotočeno je na sigurnost, učinkovitost, imunoinformatiku te proizvodnju i isporuku cjepiva: bibliometrijska analiza temeljena na VOSvieweru. Biosci Trendovi. https://doi.org/10.5582/bst.2021. 01061
Choi Y, Chang J (2013) Virusni vektori za primjenu cjepiva. Clin Exp Vaccine Res 2:97.https://doi.org/10.7774/cevr.2013.2.2.97
Chowdhury MA, Hossain N, Kashem MA, Shahid MA, Alam A (2020.) Imunološki odgovor kod COVID-a-19: pregled. J Zaraziti javno zdravlje. https://doi.org/10.1016/j.jiph.2020.07.001
Coban C, Kobiyama K, Jounai N, Tozuka M, Ishii KJ (2013) DNK cjepiva: jednostavna DNK senzorna materija? Hum Vaccin Immunother 9:2216-2221.https://doi.org/10.4161/hv.25893
Conforti A et al (2022.) COVID-eVax, kandidat za elektroporirano DNK cjepivo koje kodira SARS-CoV-2 RBD, izaziva zaštitne reakcije na životinjskim modelima. Mol Ther 30:311–326. https://doi. org/10.1016/j.ymthe.2021.09.011
Conforti A, Sanchez E, Salvatori E, Lione L, Compagnone M, Pinto E et al (2023) Linearni DNK kandidat za cjepivo koji kodira veznu domenu receptora SARS CoV-2 izaziva snažan imunološki odgovor i neutralizirajuća antitijela kod domaćih mačaka. Mol Ther-Metho Clinic Dev 28:238–248. https://doi.org/10.1016/j.omtm.2022. 12.015
Croyle M, Cheng X, Wilson J (2001.) Razvoj formulacija koje povećavaju fizičku stabilnost virusnih vektora za gensku terapiju. Gene Ther 8:1281–1290.https://doi.org/10.1038/sj.gt.3301527
Cu Y i suradnici (2013.) Poboljšana isporuka i moć samopojačavajućih mRNA cjepiva elektroporacijom in situ. Vaccines 1:367–383. https://doi.org/10.3390/vaccines1030367
