Antitirozinazna svojstva različitih vrsta kurkume i izolacija aktivnih spojeva iz Curcuma Amada
Mar 18, 2022
Jesmin Akter1 ● Md. Zahorul Islam1,2 ● Md. Amzad Hossain1 ● Kensaku Takara1
1 Poljoprivredni fakultet Sveučilišta Ryukyus, Okinawa, Japan
2 Odjel za farmakologiju, Veterinarski fakultet, Bangladeško poljoprivredno sveučilište, Mymensingh, Bangladeš
Za više informacija:Scotty.Wang@wecistanche.com
Sažetak
Kurkuma se tradicionalno koristi kao kozmetika za kožu u nekim vjerskim i kulturnim prilikama na indijskom potkontinentu. U ovoj studiji usporedili smo inhibicijska svojstva tirozinaze četiri Curcuma spp., naime C. xanthorrhiza, C. aromatic, C. amada i C. zedoaria. Izolacija i pročišćavanje inhibitora tirozinaze vođena biološkom analizom pomoću stupca silikagela i tekućinske kromatografije visoke učinkovitosti. Strukturna identifikacija spojeva provedena je pomoću 'H NMR, 13C
NMR i tekućinska kromatografija-tandem masena spektrometrija. C. amada pokazala je najveću inhibitornu aktivnost tirozinaze, s IC50 od 53,4 ug/mL. Stoga je odabran za izolaciju i pročišćavanje inhibitora tirozinaze. Pročišćeni spojevi bili su zederone (1), furanodienon (2), 1,5-epoksi-3-hidroksi-1-(3,4-dihidroksi-5-metoksifenil){ {13}}(4-hidroksifenil) heptani (3), 3,5-dihidroksi-1-(3,4-dihidroksi fenil)-7-({{22 }}hidroksi-3-metoksifenil) heptani (4) i 1,5- epoksi 3-hidroksi-1-(3,4-dihidroksi-5-metoksifenil) -7-(4-hidroksi-3-metoksifenil) heptani (5). IC50 vrijednosti za gljivuanti-tirozinazaaktivnost spojeva 1, 2, 3, 4 i 5 bila je 108,2, 89,2, 92,3, 21,7 i 41,3 uM, redom. Ovi spojevi su također inhibirali unutarstaničnu aktivnost tirozinaze, smanjujući tako sintezu melanina u stanicama melanoma B16F10. Spoj 4 pokazao se znatno jačimanti-tirozinazaaktivnost od arbutina (lijeka za pozitivnu kontrolu). Nije opažena značajna razlika u inhibicijskom učinku tirozinaze između spoja 5 i arbutina. Naša otkrića snažno sugeriraju da je C. Amanda obećavajući izvor prirodnih inhibitora tirozinaze za sprječavanje melanogeneze i da bi se mogla koristiti kao kozmetika za izbjeljivanje.
Ključna riječ: Curcuma amada ● Aktivni spojevi ● NMR ● Antitirozinaza ● Antimelanogeni

Clizati Cistanche za anti-tirozinazu
Uvod
Melanin je crni pigment u kosi i koži i neophodan je za zaštitu kože od UV zračenja. Pigment proizvode stanice melanocita, prisutne u bazalnom sloju dermisa kroz fiziološki proces koji se naziva melanogeneza. Međutim, abnormalna proizvodnja melanina uzrokuje dermatološke poremećaje kao što su pjege, melazma, lentigini, staračke pjege, efelidi i postupalna hiperpigmentacija [1]. U prehrambenoj industriji hiperpigmentacija voća i povrća dovodi do značajnih gubitaka nutritivne kvalitete i tržišne vrijednosti [2]. Melanogeneza se može kontrolirati inhibicijom aktivnosti tirozinaze, enzima koji ograničava brzinu sinteze melanina u sisavaca, biljaka, mikroorganizama i gljiva [3]. Stoga inhibicija aktivnosti tirozinaze sprječava hiperpigmentaciju i dovodi do izbjeljivanja kože. Također kontrolira kvalitetu povrća i voća reguliranjem neželjenog tamnjenja povrća i hrane. Većina sredstava za posvjetljivanje kože, kao što su hidrokinon, azelaična kiselina, kojična kiselina i arbutin, snažni su inhibitori tirozinaze. Međutim, imaju različite neželjene učinke kao što su citotoksičnost, okronoza, vitiligo, iritacija, ljuštenje kože i crvenilo [4]. Štoviše, kojična kiselina i -arbutin pokazuju lošu stabilnost formulacije i sposobnost prodiranja u kožu te nisku učinkovitost in vivo [5]. Neke organske i anorganske soli žive imaju antimelanogene učinke i koriste se u sredstvima za izbjeljivanje kože. Međutim, kroz kožnu apsorpciju, spojevi žive mogu izazvati toksične učinke kao što su promjena boje kože, oštećenje bubrega, alergijska reakcija i ožiljci [6]. Stoga je potrebno istraživanje manje toksičnih i učinkovitijih inhibitora tirozinaze. Kurkuma (obitelj: Zingiberaceae; rod: Curcuma), tradicionalna ljekovita biljka koja raste pretežno u tropskim i suptropskim područjima Azije i Afrike, ima širok spektar farmakoloških funkcija. Tradicionalno se koristio u predbračnim ritualima tisućama godina na indijskom potkontinentu kao sredstvo za posvjetljivanje kože. Vjeruje se da kurkuma poboljšava ten kože smanjujući rast dlaka na licu, akne i starenje kože [7, 8]. Stoga su proizvodi za njegu kože s dodatkom kurkume komercijalno dostupni na tržištu [9]. Identificirano je više od 70 vrsta/sorti kurkume s različitim kemijskim i farmakološkim svojstvima. Međutim, nedostaju znanstveni podaci o antimelanogenim svojstvima različitih vrsta kurkume i potencijalnim aktivnim komponentama prisutnim u kurkumi. Kurkuminoidi su glavni aktivni spojevi odgovorni za većinu bioloških aktivnosti kurkume. Kurkuminoidi imaju potencijal u kozmeceutici kaoantioksidans, protuupalno,i sredstvo za posvjetljivanje kože [7, 8]. Međutim, u prethodnoj studiji pronašli smo značajne varijacije u sadržaju kurkuminoida u kurkumi, a neke vrste (C. amada, C. zedoaria) nisu ni sadržavale kurkumin [10]. Također smo prijavili antimikotik,antioksidans, te vazodilatacijsko djelovanje različitih vrsta i sorti kurkume [10-13]. Stoga je ova studija imala za cilj procijeniti učinke različitih vrsta kurkume, naime C. xanthorrhiza, C. aromatica, C. amada i C. zedoaria, na enzim tirozinazu i identificirati specifične kemijske spojeve odgovorne zaanti-tirozinazaaktivnost. Također smo procijenili inhibitornu aktivnost tirozinaze i antimelanogene učinke pročišćenih aktivnih spojeva na sintezu melanina u stanicama melanoma B16F10.

Rezultati i rasprava
Među četiri različite vrste kurkume, MeOH ekstrakt C. amada pokazao je najveći inhibicijski učinak na tirozinazu gljiva s IC50 vrijednošću od 53,4 ± 2,7, a slijede ga C. xanthorrhiza, C. aromatic i C. zedoaria (Slika 1a). Kurkumin je glavna aktivna komponenta kurkume (Curcuma longa) i posjeduje širok raspon bioloških aktivnosti, uključujući antikancerogeno, protuupalno, antibakterijsko, antigljivično i antioksidativno djelovanje. Pokazao je 75-puta jače djelovanje protiv tirozinaze od arbutina i kojične kiseline [14]. Međutim, u prethodnom istraživanju izvijestili smo da postoje značajne varijacije u sadržaju kurkumina u različitim vrstama kurkume [10].

Kurkumin je bio prisutan u C. xanthorrhiza i C. aromatic, ali ga nije bilo u C. zedoaria i C. amada [10]. Zanimljivi nalazi ove studije su da je, bez kurkumina, C. amada pokazala snažno inhibitorno djelovanje na tirozinazu. Ovaj rezultat ukazuje da moraju postojati neki aktivni spojevi C. amada koji se pripisuju njegovom snažnom učinku protiv tirozinaze. Antitirozinazna aktivnost C. xanthorrhiza i C. aromatica mogla bi biti posljedica njihovog sadržaja kurkumina. Međutim, nismo mogli isključiti mogućnost prisutnosti drugih spojeva. MeOH ekstrakt C. amada je frakcioniran s vodom, n-heksanom i EtOAc. Među te tri frakcije, EtOAc je pokazao značajno jači inhibicijski učinak od vode i n-heksana (slika 1b). Zbog toga je dio EtOAc uzet za daljnje frakcioniranje. Aktivnosti protiv tirozinaze šest frakcija [n-heksan:EtOAc; 100:0 (F1), 80:20 (F2), 60:40 (F3), 40:60 (F4), 20:80 (F5) i 0:100 (F6)] iz EtOAc dijela C. amada su uspoređeni. Među tih šest frakcija, F6 i F3 pokazale su značajno veću aktivnost protiv tirozinaze od ostalih (slika 1c). Zatim su identificirane kemijske strukture pet spojeva iz frakcija F3 i F6 prema njihovim 1H NMR i 13C NMR spektrima. Vršni podaci bili su sljedeći:

Spoj 1:
Bezbojni igličasti kristal; UV λmax: nm 234, 285. ESI-MS (plus) m/z: 247,3 [M plus H] plus, 229,4 [M plus H-H2O] plus. 'H-NMR (CD3OD): 8 7,22 (1H, s, H-12), 5,59 (1H, br d, J=12 Hz, H{{20}}) 3,99 (1H, s, H-5), 3,85 (1H, d, J=16 Hz, H-9a), 3,69 (1H, d, J=16 Hz, H-9b), 2,57 (1H, dddd, J=13, 13, 12, 4 Hz, H-2a), 2,26 (1H, m, H{{46 }}a), 2,20 (1H, m, H{{50}}b), 2,09 (3H, s, H-13), 1,57 (3H, s, H-15), 1,32 (IH, ddd, J=13, 13, 4 Hz, H-3b), 1,28 (3H, s, H-14). 13C-NMR (CD3OD): 8 194,2 (C-6) 160,2 (C-8), 139,7 (C12), 132,8 (C-1), 132,0 (C-10) ), 124.3(C-11), 123.0(C-7), 67.8(C-5), 65.2(C-4), 42.5(C-9 ), 39,0(C-3), 25,4(C-2), 15,7 (C-15), 15,4(C-14), 10,7(C-13 ) (dodatni podaci). Usporedbom ovih podataka s onima objavljenima u literaturi [15, 16], tvar je identificirana kao zederone (slika 2). To je seskviterpen, prethodno je izoliran iz C. amada i C. zedoaria, a objavljeno je zbog njegovih analgetskih, protuupalnih, antifungalnih i citotoksičnih učinaka [12, 17-20].
Spoj 2:
Bezbojno ulje; UV λmax: nm 243, 280. ESIMS (plus) m/z: 231.0 [M plus H] plus, 223,3 [M plus H-H2O] plus. 'H-NMR (CD3OD): 8 7,16 (1H, s, H-12), 5,83 (1H, s, H-5), 5,21 (1H, dd, J=12 Hz , 5 Hz, H-1), 3,73 (1H, d, J=16 Hz, H-9a), 3,63 (1H, d, J=16 Hz, H -9b), 2,45 (1H, ddd, J=15 Hz, 11 Hz, 4 Hz, H-3a), 2,31 (1H, m, H-2a ), 2,20 (1H, dddd, J=12 Hz, 12 Hz, 12 Hz, 4 Hz, H-2b), 2,06 (3H, s, H{{57} }), 1,92 (3H, s, H-14), 1,89 (1H, m, H-3b), 1,25 (3H, s, H-15). 13C-NMR (CD3OD): 8 191,8 (C-6), 158,6 (C-8), 147,6 (C-4), 140,0 (C-12), 136,1 ( C-10), 133,3 (C-5), 132,0 (C-1), 124,6 (C-11), 123,1 (C-7), 42,4 ( C-9), 41,4 (C-3), 27,3 (C-2), 19,3 (C-14), 15,9 (C-2), 9,9 ( C-13) (dodatni podaci). Usporedbom ovih podataka s onima objavljenima u literaturi [21], tvar je identificirana kao furanodienon (slika 2). Izoliran je iz Lindera pulcherrima (Nees.) Benth. ex kuka. f [22], Curcuma zedoaria [19], Curcuma amada [12] i Curcuma wenyujin [23]. To je furanoseskiterpenoid koji pokazuje antigljivične [12], protuupalne [19], antikancerogene [24], antibakterijske i antioksidativne aktivnosti [22].
Spoj 3:
Žućkasto ulje; UV λ max: nm 275. ESIMS (plus) m/z: 383,3 [M plus Na] plus, 361,3 [M plus H] plus, 343,2 [M plus H-H2O] plus. 'H-NMR (CD3OD): 5 6,99 (2H, dd, J=9, 2 Hz, H-2´´, -6´´), 6,67 (2H, d, J=9 Hz, H-3´´, -5´´), 6,52 (2H, s, H-2´, -6´), 4,63 (1H , br b, J=12 Hz, H-1), 4,21 (1H, m, H-3), 3,89 (1H, m, H-5), 3,85 ( 3H, s, 5´-OCH3), 2,63 (2H, m, H-7), 1,82 (1H, m, H-2a), 1,78 (1H, m, H{{6{ {107}}}a), 1,73 (1H, m, H-2b), 1,69 (1H, m, H-4a), 1,68 (1H, m, H{{72} }b), 1,53 (IH, m, H-4b). 13C-NMR (CD3OD): 8 156,3 (C-4´´), 149,5 (C-5´), 146,4 (C-3´), 134,5 (C-4 ´), 134,44 (C-1´), 134,41 (C-1´´), 130,4 (C-2´´, -6´´), 116,1 (C{ {104}}´´, -5´´), 108,0 (C-2´), 102,8 (C-6´), 75,2 (C-1), 72,6 ( C-5), 65,6 (C3), 56,6 (5´-OCH3), 41,1 (C-2), 39,5 (C-4), 39,2 (C-6) 31.8 (C-7) (Dodatni podaci). Usporedbom ovih podataka s onima objavljenim u literaturi [25], tvar je identificirana kao 1,5-epoksi-3-hidroksi-1-(3,4-dihidroksi{ {145}} metoksifenil)-7-(4-hidroksifenil) heptani (Slika 2). Izoliran je iz rizoma Zingiber officinale, te su proučavana njihova antioksidativna svojstva [25].
Spoj 4:
Viskozni sirup; UV λ max: nm 281. ESIMS (plus) m/z: 385,3 [M plus Na] plus, 363,3 [M plus H] plus, 345,2 [M plus H-H2O] plus. 'H-NMR (CD3OD): 5 6,75 (1H, d, J=2 Hz, H-2´), 6,68 (1H, d, J=8 Hz, H{{21 }}´), 6,64 (1H, J=8 Hz, H-5´´), 6,61 (1H, J=2 Hz, H-2´´), 6,60 (1H, dd, J=8, 2 Hz, H-6´), 6,49 (1H, dd, J=8, 2 Hz, H-6´´), 3,80 (3H, s, 3´-OCH3), 3,73 (2H, m, H-3, -5), 2.64-2.47 (4H, m, H{{59) }}a, -1b, -7a, -7b), 1.71-1.65 (4H, m, H-2a, {{ 68}b, -6a, -6b), 1,61 (2H, m, H-4a, -4b). 13C-NMR (CD3OD): 8 148,8 (C-3´), 146,1 (C-3´´), 145,4 (C-4´), 144,2 (C-4 ´´), 135,24 (C-1´ ili C-1´´), 135,22 (C-1´ ili C-1´´), 121,8 (C{{101 }}´), 120,6 (C-6´´), 116,5 (C-2´´), 116,3 (C-5´´), 116,1 (C-5´ ), 113,2 (C-2´), 70,94 (C-3 ili C-5), 70,92 (C-3 ili C-5), 56,4 (3 ´-OCH3), 44,9 (C-4), 40,8 (C-2, -6), 32,3 (C-1), 32,1 (C-7) (Dodatni podaci). Usporedbom ovih podataka s onima objavljenim u literaturi [26, 27], tvar je identificirana kao ulje 3,5-dihidroksi-1-(3,4-dihidroksifenil){{150 }} (4-hidroksi-3-metoksifenil) heptani (Slika 2). Izoliran je iz rizoma Tacca chantrieri [26] i Curcumalonga L. [27]. Oni su diarilheptanoidi koji pokazuju citotoksično [26] i antitumorsko [27] djelovanje.
Spoj 5:
Bezbojno ulje; UV λ max nm: 279. ESI-MS (plus) m/z: 413,3 [M plus Na] plus, 391,3 [M plus H] plus, 373,3 [M plus HH2O] plus. 'H-NMR (CD3OD): 5 6,76 (1H, s, H-2´´), 6,67 (1H, d, J=8 Hz, H{{20}} ´´), 6,21 (1H, dd, J=8, 2 Hz, H-6´), 6,53 (2H, s, H-2´, -6´´ ), 4,63 (1H, br d, J=12 Hz, H-1), 4,21 (1H, m, H-3), 3,83 (3H, s, 5´-OCH3) 3,78 (3H, s, 3-OCH3), 2,65 (2H, m, H-7), 1,84 (1H, m, H-2a), 1,79 (1H, m, H-6a), 1,74 (1H, m, H-2b), 1,69 (1H, m, H-4a), 1,68 (1H, m, H{{ 75}}b), 1,53 (IH, m, H-4b). 13C-NMR (CD3OD): 8 149,5 (C-5´), 148,8 (C-3´´), 146,4 (C-3´), 145,4 (C-4 ´´), 135,3 (C-1´), 135,2 (C-1´´), 134,4 (C-4´), 121,9 (C-6´´), 116,1 (C-5´´), 113,4 (C-2´´), 108,0 (C-2´), 102,7 (C-6´), 75,2 (C{ {121}}), 72,5 (C-5), 65,6 (C-3), 56,6 (5´-OCH3), 56,3 (3´´-OCH3), 41,2 (C{{140} }), 39.4 (C-4), 39.3 (C-6), 32.2 (C-7) (Dodatni podaci). Usporedbom ovih podataka s onima navedenima u literaturi [20], tvar je identificirana kao 1,5-epoksi-3-hidroksi-1-(3,4-dihidroksi{ {157}}metoksifenil)- 7-(4-hidroksi-3-metoksifenil) heptani (Sl. 2) i nema informacija o njihovoj biološkoj aktivnosti. Spojeve 3, 4 i 5 smo prvi put izolirali iz C. amada. Svi spojevi su pokazali inhibicijsku aktivnost protiv tirozinaze gljiva
Pet spojeva, naime, zederone, furanodienon, 1,5-epoksi-3-hidroksi-1-(3,4-dihidroksi-5-metoksifenil)- 7-( 4-hidroksifenil) heptani, 3,5-dihidroksi-1-(3,4-dishi hidroksifenil)-7-(4-hidroksi-3- metoksifenil) heptani i 1,5-epoksi-3-hidroksi-1-(3,4-dihidroksi-5-metoksifenil)- 7-(4- hidroksi-3-metoksifenil) heptani, izolirani su iz frakcija F3 i F6. Izolirani spojevi pokazali su aktivnost protiv tirozinaze na način ovisan o koncentraciji. Među pet spojeva, spoj 4 pokazao je znatno jače djelovanje protiv tirozinaze od arbutina. Nije bilo značajnih razlika u učincima protiv tirozinaze između spoja 5 i arbutina (slika 3). Učinci izoliranog spoja na staničnu vitalnost proučavani su na stanicama mišjeg melanoma B16F10. Stanice su tretirane s koncentracijama spoja od 50, 100, 200 i 400 µM tijekom 48 sati. Izolirani spojevi nisu pokazali citotoksične učinke do 200 µM, međutim, oko pedeset posto staničnih smrti uočeno je u svim slučajevima pri koncentraciji od 400 µM (slika 4). Stoga su koncentracije do 200 µM korištene za procjenu njihovih intracelularnih antitirozinaznih i antimelanogenih učinaka.


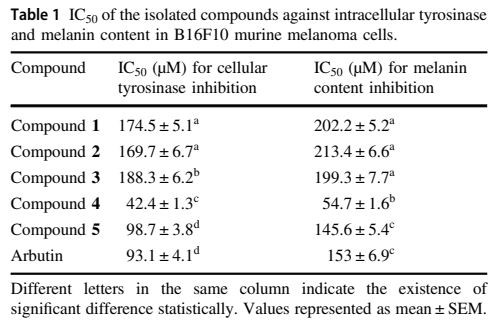
Kako bi se odredila antimelanogena i antitirozinazna aktivnost izoliranih spojeva, procijenjeni su njihovi učinci na sadržaj melanina i aktivnost tirozinaze u stanicama melanoma B16F10. Kao što je prikazano u tablici 1, naši izolirani spojevi ovisno o dozi inhibirali su intracelularni sadržaj melanina i aktivnost tirozinaze. Spoj 4 bio je značajno jači od pozitivnog kontrolnog lijeka arbutina u inhibicijskim učincima melanina i tirozinaze. Nije uočena značajna razlika između spoja 5 i arbutina. Kako stanična tirozinaza pojačava proizvodnju melanina, smanjenje aktivnosti tirozinaze učinkovita je strategija za razvoj antimelanogenih sredstava. Za to smo procijenili inhibitorna svojstva intracelularne aktivnosti tirozinaze i melanogeneze u stanicama melanoma B16F10. Slično nalazima inhibitorne aktivnosti tirozinaze gljiva, izolirani spojevi inhibiraju unutarstaničnu aktivnost tirozinaze i melanogenezu na način ovisan o dozi. Antitirozinazni učinci izoliranih spojeva rezultirali su njihovim antimelanogenim svojstvima. Redoslijed antitirozinazne i antimelanogene aktivnosti ovih spojeva bio je spoj 4 > arbutin > 5 > 2 > 3 > 1. Izračunata vrijednost IC50 spoja 4 bila je značajno niža od one za arbutin. Učinkovitost spoja 4 bila je 1.9- do 5-puta veća od učinkovitosti ostala četiri spoja. Spoj 5 je također pokazao snažnu aktivnost protiv tirozinaze koja je bila usporediva s onom arbutina. Naši rezultati pokazuju da se spojevi 4 i 5 mogu koristiti kao potencijalni prirodni inhibitori tirozinaze i kozmetika za izbjeljivanje kože. Pretpostavlja se da je oksidativni stres uključen u temeljni mehanizam prekomjerne proizvodnje melanina [28]. Stoga je uloga antioksidansa istražena u širokom rasponu kožnih poremećaja, uključujući fotokarcinogenezu ili melanom [9]. Mi i drugi prethodno smo izvijestili o antioksidativnim svojstvima C. amada [13, 29] koja bi mogla biti odgovorna za antimelanogene učinke izoliranih spojeva. U ovoj smo studiji otkrili inhibitorne učinke izoliranih spojeva na intracelularnu sintezu melanina i aktivnost tirozinaze induciranu s -MSH. Stoga se naši izolirani spojevi mogu koristiti kao sredstva u funkcionalnoj kozmetici za razvoj učinkovitih tretmana za izbjeljivanje kože.

Zaključak
Čvrsto predlažemo da C. amada može igrati važnu ulogu kao učinkovit inhibitor tirozinaze. C. amada i njezini bioaktivni spojevi mogu se koristiti u kozmetičkoj industriji kao prirodna sredstva za izbjeljivanje, u prehrambenoj industriji kao sredstva protiv posmeđivanja i u medicini za liječenje hiperpigmentacije. Unatoč tome, potrebna su daljnja istraživanja kako bi se istražili antimelanogeni učinci izoliranih spojeva na životinjskim modelima.
Materijali i metode
Kemikalije
Tirozinaza iz gljiva i arbutin nabavljeni su od Sigma–Aldrich Chemical Co. (St. Louis, MO, SAD). L-Tirozin je bio iz Wako pure chemical industries Ltd. (Osaka, Japan). Metanol (MeOH), etil acetat (EtOAc) i n-heksan nabavljeni su od Nacalai Tesque (Kyoto, Japan). Kupljeni su silikagel (63–200 μm, Kanto Chemical Co. Tokyo, Japan) i MeOH-d4 (CD3OD, Merck KGaA, Njemačka).
Priprema biljnog materijala Četiri različite vrste kurkume, naime C. xanthorrhiza, C. aromatica, C. amada i C. zedoaria, uzgajane su na polju sivog tla (krupni pijesak 3,6 posto, fini pijesak 30,9 posto , mulj 24,3 posto, glina 32,8 posto, pH 7,4, NO{{10}}N 0,07 posto, NH4-N 0,08 posto, P 4,6 ng/g, K 42,9 ng/g) na Subtropical Field Science Center, Sveučilište Ryukyus, Okinawa, Japan. Prosječna mjesečna temperatura, vlažnost i oborina tijekom razdoblja uzgoja bile su 17-29 stupnjeva, 61-83 posto, odnosno 22-369 mm. Osigurane su uobičajene agronomske prakse uključujući gnojivo i navodnjavanje. Rizomi su sakupljeni kada su svi izdanci vrste potpuno uvenuli. Rizomi su oprani, narezani i osušeni u pećnici s vrućim zrakom na 50 stupnjeva 72 sata.
Ekstrakcija uzoraka
Ekstrakcije su provedene otapanjem različitog praha kurkume (300 g) u MeOH (3 L) na sobnoj temperaturi (25 stupnjeva) i atmosferskom tlaku i držane dva dana uz kontinuirano magnetsko miješanje kako bi se spriječila oksidacija zrakom i zaštitilo od sunčeve svjetlosti. Spojevi topivi u otapalu su filtrirani korištenjem filter papira (br. 2, Advantec, Tokyo Roshi Kaisha Ltd., Tokyo, Japan). Iskorištenom biljnom materijalu dodana su svježa otapala (MeOH) i postupak je ponovljen tri puta. Filtrirane otopine koje sadrže biljne spojeve su osušene pomoću rotacijskog isparivača pod smanjenim tlakom na 40 stupnjeva. Prinos svih ekstrakata držan je u hladnjaku na 4 stupnja za eksperimentalne analize.

Test inhibicije tirozinaze
Aktivnost inhibicije tirozinaze određena je prema prethodnoj metodi [30], mjerenjem koncentracije DOPA kroma proizvedenog djelovanjem enzima tirozinaze na tirozinski supstrat. Ukratko, testni uzorak je otopljen u 80 posto MeOH da se dobiju različite koncentracije (25, 50 i 100 µg/mL). 96-Ploča s jažicama postavljena je sljedećim redoslijedom: 120 μL fosfatnog pufera (20 mM, pH 6,8), 20 μL uzorka i 20 μL tirozinaze gljive (500 U/mL u 20 mM fosfata pufer). Nakon inkubacije od 15 minuta na 25 stupnjeva, reakcija je započeta dodavanjem 20 μL 0,85 mM otopine L-tirozina i zatim je inkubirana 10 minuta na 25 stupnjeva. Aktivnost tirozinaze određena je mjerenjem apsorbancije na 470 nm pomoću čitača mikropločica (Biotek Powerwave XS2 spektrofotometar). Arbutin je korišten kao pozitivna kontrola, dok je 80-postotni MeOH korišten kao negativna kontrola. Postotak inhibicije tirozinaze izračunat je na sljedeći način:

gdje je C apsorbancija negativne kontrole, B je apsorbancija slijepe probe, a S je apsorbancija ispitnog uzorka.

Izolacija bioaktivnih spojeva iz sirovog ekstrakta Curcuma amada
Uzimajući u obzir rezultate četiriju ekstrakta kurkume, C. amada je pokazala značajno veću aktivnost protiv tirozinaze od ostalih. Stoga je provedeno pročišćavanje aktivnih spojeva iz sirovog ekstrakta C. amada vođeno biološkim testom. Kako bi se identificirali spojevi protiv tirozinaze, provedeno je frakcioniranje iz sirovog ekstrakta C. amada kako je opisano na slici 5. Sirovi ekstrakt je razrijeđen destiliranom vodom i zatim ekstrahiran n-heksanom, a zatim EtOAc. Jednaki volumeni svakog otapala i otopine sirovog ekstrakta zatim su pomiješani mućkanjem 3 minute u lijevku za odjeljivanje. Sve frakcije su koncentrirane do suhog pomoću rotacijskog isparivača na 40 stupnja. Aktivnosti protiv tirozinaze ove tri frakcije određene su prema gornjem postupku. Budući da je EtOAc frakcija pokazala najveću aktivnost protiv tirozinaze, odabrana je za izolaciju i pročišćavanje bioaktivnog spoja. Aktivna EtOAc frakcija je uparena do suhoće i podvrgnuta kromatografiji na stupcu silikagela (75 g) (30 × 3 cm). Elucija je provedena upotrebom n-heksana i EtOAc s rastućim količinama EtOAc [100:0 (F1), 80:20 (F2), 60:40 (F3), 40:60 (F4), 20:80 (F5) , i 0:100 (F6)]. Antitirozinazna aktivnost ovih šest frakcija provedena je u skladu s gornjim postupkom, a većina aktivnosti je nađena u F3 i F6. Frakcije F3 i F6 pročišćene su pomoću C18 HPLC reverzne faze (COSMOSIL 5C18-AR-II; Nacalai Tesque, Inc., Kyoto, Japan) opremljene vodom i acetonitrilom kao mobilnom fazom s brzinom protoka od 2,5 mL min−1, detektirano na 280 nm.
Tri pika iz F3 eluirana su na 9,55, 13,66 i 16,47 minuta, a četiri pika iz F6 eluirana su na 11,56, 12,20, 12,75 i 15.03 minute kao bezbojne bijele tvari, od kojih inhibitorne aktivnost je detektirana u pet vršnih frakcija eluiranih na 9,55 i 16,47 min iz F3 i 11,56, 12,75 i 15.03 min (dodatni podaci) iz F6 (Slika 5). Izolirani spojevi (~10 mg) su otopljeni u MeOH-d4 i zatim podvrgnuti spektralnoj analizi. Spektri nuklearne magnetske rezonancije (NMR) snimljeni su na BRUKER NMR spektrometrima (500 MHz za 1 H i 125 MHz za 13 C) na sobnoj temperaturi. Kemijski pomaci (δ) zabilježeni su kao dijelovi na milijun (ppm) u odnosu na tetrametilsilan (TMS) kao interni standard. Eksperimenti masene spektrometrije provedeni su na Watersovom spektrometru mase upotrebom sonde za elektrosprej ionizaciju (ESI − MS) pod sljedećim instrumentalnim uvjetima: Kolona: COSMOSIL 5C18-AR-II, (2 × 150) mm. Otapalo A: voda (0,1 posto mravlja kiselina), otapalo B: acetonitril, brzina protoka: 4 mL/min, volumen ubrizgavanja: 100 µL, vrijeme rada: 35 min, vremenski program za F3: 75 posto B (0 min) → 75 postotak B (20 min) → 100 posto B (20,1 min) → 100 posto B (27 min) → 75 posto B (27,1 min) → 75 posto B (35 min). Vremenski program za F6: 45 posto B (0 min) → 45 posto B (14 min) → 100 posto B (14,1 min) → 100 posto B (20 min) → 45 posto B (20,1 min) → 45 posto B (25 min). Način pumpanja: Binarni gradijent. Detalji pećnice: CTO-20AC, temperatura 40 stupnjeva. MS ionizacijski mod: ES (plus), kapilarni napon: 4,0 kV, konusni napon: 20 V, temperatura izvora: 120 stupnjeva, temperatura desolvatacije: 350 stupnjeva, protok konusnog plina: 100 L/h, protok plina desolvatacije: 800 L /h (dodatni podaci).
Antitirozinazna aktivnost izoliranih spojeva
Izolirani spojevi otopljeni su u MeOH u koncentracijama od 5, 10, 30, 50, 100 i 200 μM za svaki spoj. Aktivnost protiv tirozinaze određena je primjenom prethodno opisanog postupka.

Intracelularna inhibicija tirozinaze i melanogeneze izoliranim spojevima
Kultura stanica
Stanice melanoma B16F10 uzgajane su u Dulbecco-ovom modificiranom Eagleovom mediju (DMEM) s dodatkom 10 posto toplinski inaktiviranog fetalnog goveđeg seruma (FBS) i 1 posto penicilina (10,000 U/mL)/streptomicina (100 ug/mL) na 37 stupnjeva u vlažnoj atmosferi koja sadrži 5 posto CO2.
Viabilnost stanica
B16F10 stanice su nasađene u gustoći od 5 × 104 stanica/jažici u 96-ploču s jažicama. Nakon 24 sata, stanice su bile izložene različitim koncentracijama izoliranog spoja i inkubirane dodatnih 48 sati na 37 stupnjeva. Nakon inkubacije, viabilnost stanica određena je MTS testom. Dodano je dvadeset mikrolitara MTS otopine i inkubirano 60 minuta. Nakon inkubacije, apsorbancija stanica određena je na 490 nm pomoću čitača mikropločica (Benchmark Plus).
Antitirozinazno i antimelanogeno djelovanje izoliranih spojeva
Određivanje sadržaja melanina u stanici i testovi aktivnosti tirozinaze provedeni su kao što je prethodno opisano [31], uz male modifikacije. Stanice melanoma B16F10 nasađene su u gustoći od 5 × 104 stanica/jažici u 96-ploču s jažicama. Nakon 24 sata stanice su bile izložene različitim koncentracijama izoliranog spoja ili arbutina. Nakon 1 h, dodano je 100 nM -melanocit-stimulirajućeg hormona (-MSH), a stanice su inkubirane dodatnih 48 h na 37 stupnjeva. Za ispitivanje aktivnosti protiv tirozinaze, stanice su zatim isprane ledeno hladnim fosfatnim puferom i lizirane fosfatnim puferom (pH 6,8) koji je sadržavao 1 posto Triton-X (90 μL/jažici). Ploče su bile zamrznute na -80 stupnjeva 30 minuta. Nakon odmrzavanja i miješanja, u svaku jažicu je dodano 10 μL 1 posto L-DOPA. Nakon inkubacije na 37 stupnjeva tijekom 2 sata, apsorbancija je izmjerena na 490 nm. Za analizu sadržaja melanina, stanice su dva puta isprane fosfatnim puferom i zatim otopljene u 100 μL NaOH (1 N) koji sadrži 10 posto DMSO. Uzorci su inkubirani na 80 stupnjeva 1 h i pomiješani kako bi se otopio melanin. Optička gustoća miješanog homogenata izmjerena je na 490 nm.
Statistička analiza
Rezultati su izraženi kao srednja vrijednost ± SEM. Statističke razlike između dvije srednje vrijednosti procijenjene su Studentovim t-testom. Višestruke usporedbe provedene su korištenjem jednosmjerne analize varijance praćene Bonferronijevim testom. Razlike su se smatrale značajnim pri P <>
Ovo je naš proizvod protiv umora! Kliknite na sliku za više informacija!
Reference
1. Solano F, Briganti S, Picardo M, Ghanem GH. Hipopigmentirani agensi: ažurirani pregled bioloških, kemijskih i kliničkih aspekata. Pigment Cell Res. 2006;19:550–71.
2. Loizzo MR, Tundis R, Menichini F. Prirodni i sintetski inhibitori tirozinaze kao sredstva protiv smeđivanja: Ažuriranje. Compr Rev Food Sci Food Saf. 2012;11:378–98.
3. Lin YS, Chen HJ, Huang JP, Lee PC, Tsai CR, Hsu TF, et al. Kinetika inhibitorne aktivnosti tirozinaze korištenjem ekstrakata lista vinifere Viti. Biomed Res Int. 2017: 5232680.
4. Manini P, Napolitano A, Westerhof W, Riley PA, d' Ischia M. Reaktivni orto-kinon generiran oksidacijom agensa za depigmentaciju kože monobenzona kataliziranom tirozinazom: reakcije samospajanja i tiolne konjugacije i moguće implikacije za melanocite toksičnost. Chem Res Toxicol. 2009;13:1398-405.
5. Couteau C, Coiffard L. Pregled sredstava za izbjeljivanje kože: lijekovi i kozmetički proizvodi. Kozmetika. 2016;3:27.
6. Al-Saleh I, Shinwari N, El-Doush I, Billedo G, Al-Amodi M, Khogali F. Usporedba razine žive u različitim tkivima albino i pigmentiranih miševa tretiranih s dvije različite marke živinih krema za posvjetljivanje kože. Biometali: Int J uloga Met ioni Biol, Biochem, Med. 2004;17:167–75.
7. Gopinath H, Karthikeyan K. Kurkuma: začin, kozmetika i lijek. Indijski J Dermatol Venereol Leprol. 2018;84:16–21.
8. Vaughn AR, Branum A, Sivamani RK. Učinci kurkume (Curcuma longa) na zdravlje kože: sustavni pregled kliničkih dokaza. Phytother Res. 2016;30:1243-64.
9. Baliga MS, Katiyar SK. Kemoprevencija fotokarcinogeneze odabranim biljnim prehrambenim proizvodima. Photochem Photobio Sci. 2006;5:243–53.
10. Akter J, Hossain MA, Sano A, Takara K, Islam MZ, Hou DX. Antifungalna aktivnost različitih vrsta i sojeva kurkume (Curcuma spp.) protiv Fusarium Solani Sensu Lato. Pharm Chem J. 2018;52:292–7.
11. Akter J, Islam MZ, Hossain MA, Kawabata S, Takara K, Nguyen H, et al. Relaksacija svinjske cerebralne arterije neovisna o endotelu i o kalcijevim kanalima različitim vrstama i sojevima kurkume. J Tradit Complement Med. 2018;9:297-303.
12. Akter J, Takara K, Islam MZ, Hossain MA, Sano A, Hou DX. Izolacija i strukturno objašnjenje antifungalnih spojeva iz Curcuma amada. Azijski Pac J Trop Med. 2019;12:123–9.
13. Akter J, Hossain MA, Takara K, Islam MZ, Hou DX. Antioksidativno djelovanje različitih vrsta i sorti kurkume (Curcuma spp): Izolacija aktivnih spojeva. Comp Biochem Physiol C Toxicol Pharm. 2019;215:9-17.
14. Khunlad P, Tundulawessa Y, Supasiri T, Chutrtong W. Inhibicijska aktivnost tirozinaze kurkuminoida iz praha kurkume (Curcuma longa Linn.). J SWU Sci. 2008;24:125-39.
15. Giang PM, Son PT. Izolacija seskviterpenoida iz rizoma vijetnamske kurkume aromatične Salisb. J Chem. 2000;38:96-9.
16. Asem SD, Laitonjan SW. Istraživanje odnosa strukture i nelinearnosti zederona iz rizoma Curcuma caeca Roxb. Ind J Chem. 2012;51:1738–42.
17. Faiz Hossain C, Al-Amin M, Rahman KM, Sarker A, Alam MM, Chowdhury MH, et al. Analgetsko načelo iz Curcume amade. J Ethnopharmacol. 2015;163:273–7.
18. Ahmed Hamdi OA, Syed Abdul Rahman SN, Awang K, Abdul Wahab N, Looi CY, Thomas NF, Abd Malek SN. Citotoksični sastojci iz rizoma Curcuma zedoaria. Sci World J. 2014;2014:321943.
19. Makabe H, Maru N, Kuwabara A, Kamo T, Hirota M. Protuupalni seskviterpeni iz Curcuma zedoaria. Nat Prod Res. 2006;20:680–5.
20. Kikuzaki H, Nakatani N. Ciklički diarilheptanoidi iz rizoma Zingiber officinale. Fitokemija. 1996;43:273-7.
21. Dekebo A, Dagne E, Sterner O. Furanosesquiterpenes iz Commiphora sphaerocarpa i srodni pretvornici prave smirne. Fitoterapija. 2002;73:48-55.
22. Joshi SC, Mathela CS. Antioksidativno i antibakterijsko djelovanje eteričnog ulja lista i njegovih sastojaka furanodienona i curzerenona iz Lindera pulcherrima (Nees.) Benth. ex kuka. f. Pharmacogn Res. 2012;4:80–4.
23. Yang FQ, Li SP, Zhao J, Lao SC, Wang YT. Optimizacija GC-MS uvjeta na temelju rezolucije i stabilnosti analita za istovremeno određivanje devet seskviterpenoida u tri vrste rizoma kurkume. J Pharm Biomed Anal. 2007;43:73–82.
24. Li YW, Zhu GY, Shen XL, Chu JH, Yu ZL, Fong WF. Furanodienon inhibira staničnu proliferaciju i preživljavanje supresijom ER signalizacije u MCF-7 stanicama raka dojke kod ljudi. J Cell Biochem. 2011;112:217–24.
25. Tao QF, Xu Y, Lam RY, Schneider B, Dou H, Leung PS, et al. Diarilheptanoidi i monoterpenoid iz rizoma Zingiber officinale: antioksidativna i citoprotektivna svojstva. J Nat Prod. 2008;71:12-17.
26. Yokosuka A, Mimaki Y, Sakagami H, Sashida Y. Novi diarilheptanoidi i diarilheptanoidni glukozidi iz rizoma Tacca chantrieri i njihova citotoksična aktivnost. J Nat Prod. 2002;65:283–9.
27. Jiang JL, Jin XL, Zhang H, Su X, Qiao B, Yuan YJ. Identifikacija antitumorskih sastojaka u kurkuminoidima iz Curcuma longa L. na temelju odnosa sastav-aktivnost. J Pharm Biomed Anal. 2012;70:664–70.
28. Marrot L, Meunier JR. Fotooštećenje DNA kože i njegove biološke posljedice. J Am Acad Dermatol. 2008;58:139–48.
29. Policegoudra RS, Abiraj K, Channe Gowda D, Aradhya SM. Izolacija i karakterizacija antioksidativnog i antibakterijskog spoja iz rizoma manga đumbira (Curcuma amada Roxb.). J Chromatogr B Anal Technol Biomed Life Sci. 2007;852:40-8.
30. Tadtong S, Viriyaroj A, Vorarat S, Nimkuntat S, Suksamrarn S. Antitirozinaza i antibakterijske aktivnosti ekstrakta perikarpa mangostina. J Health Res. 2009;23:99-102.
31. Li X, Guo L, Sun Y, Zhou J, Gu Y, Li Y. Baicalein inhibira melanogenezu putem aktivacije ERK signalnog puta. Int J Mol Med. 2010;25:923–7.

